Allium Vegetable Research Center, National Institute of Horticultural and Herbal Science, Rural Development Administration, Muan 58545, Korea
*Correspondence to support06@korea.kr
Korean Journal of Mycology (Kor J Mycol) 2025 December, Volume 53, Issue 4, pages 237-243.
https://doi.org/10.4489/kjm.2025.53.4.1
Received on October 17, 2025, Revised on November 10, 2025, Accepted on November 10, 2025, Published on December 31, 2025.
Copyright © The Korean Society of Mycology.
This is an Open Access article which is freely available under the Creative Commons Attribution-Non-Commercial 4.0 International License (CC BY-NC) (https://creativecommons.org/licenses/by-nc/4.0/).
Fungal pathogens cause major problems in crop production by reducing crop yield and quality during growth and storage. This study evaluated the occurrence of fungal pathogens in onion bulbs (Allium cepa L.) and identified pathogenic fungal species using morphological and molecular analyses. Onion samples were collected from 20 onion-cultivated fields and stored in Muan, Hamyang, and Changnyeong. Most onion samples were contaminated with Aspergillus (49.5±36.3%), followed by Fusarium (27.2±27.4%) and Penicillium (4.9 ± 4.4%). The extent of fungal contamination varied among cultivars. Red and yellow onions were predominantly contaminated with Aspergillus (6.0–100%), whereas white onions showed a higher prevalence of Fusarium (50.0–73.3%). A total of 174 fungal colonies were isolated from onion samples, containing mainly A. welwitschiae (42.0%), followed by F. proliferatum (24.8%), P. brasilianum (6.3%), P. glabrum (5.2%), F. oxysporum (4.6%), F. commune (2.3%), A. montevidensis, and P. brevicompactum. Notably, A. welwitschiae (94.8%) and F. proliferatum (72.9%) were the most prevalent species within the genera Aspergillus and Fusarium, respectively. Other genera including Bipolaris, Chaetomium, Circinella, Cladosporium, Coprinellus, Curvularia, and Talaromyces, were also detected. These findings can serve as a tool for developing control strategies to protect onion crops against plant pathogenic fungi during cultivation and storage. Further field studies using various cultivars are required.
Aspergillus, Fungal diversity, Fusarium, Onion bulb, Penicillium
양파(Allium cepa L.)는 세계적으로 가장 광범위하게 재배되는 주요 채소 작물 중 하나로, 2023년 기준 약 22만 ha의 재배 면적에서 연간 약 500만 톤이 생산되고 있다[1]. 한국은 세계 5위의 양파 생산국으로, 연간 약 118만 톤을 생산하며[2], 양파는 국내 주요 채소 산업에서 주요한 경제 작물로 자리매김하고 있다. 국내 양파 재배는 수확 후 장기 저장 및 유통을 전제로 하는 작형 체계를 기반으로 하며, 노지재배 후 수확·건조·저장을 거쳐 신선 소비뿐 아니라 종구(seed bulb) 생산에도 이용된다. 그러나 저장, 유통 단계에서 발생하는 구(bulb) 부패는 단순한 물량 손실에 그치지 않고, 상품 품질 저하, 선별·포장·유통 비용 증가, 상품성 및 경쟁력 감소 등 생산·유통망 전반에 걸친 경제적 부담을 초래한다[3]. 특히 저장 병해는 수확 이전에 이미 구근에 침입하여 잠복해 있던 병원체가 저장 환경에서 발현되는 것이 주요 요인이며[4,5], 수확기에 구조적으로 취약한 수확기 목(neck) 조직은 병원성 미생물의 침입에 민감하다[6]. 따라서 양파 병해 관리는 재배기간 전반에 걸쳐 중요하지만, 수확기 양파 구의 건전성을 확보하는 것은 저장성 향상과 저장 병해 발생 최소화를 위한 가장 중요한 관리 단계로 평가된다.
기존 연구와 현장 관리 지침은 주로 저장·유통 단계의 구 부패에 초점을 두고 있으며[5,7,8], 양파 구의 곰팡이 다양성 연구 또한 특정 저장 병해를 유발하는 개별 병원균 중심으로 수행되어 왔다. 대표적으로, Fusarium basal rot은 저장 중 부패의 50%를 차지할 정도로 세계 각지의 양파 주산지에서 가장 파괴적인 병 중 하나로 분류되었으며[9], Fusarium oxysporum이 오랫동안 대표적인 원인균으로 알려져왔다. 그러나 최근 분자생물학적 동정 기법의 발전에 따라 F. proliferatum, F. commune, F. acuminatum, F. solani 등 다양한 Fusarium 종들이 병 발생기작에 복합적으로 관여하는 것으로 보고되고 있다[10–12]. Black mold rot 역시 Aspergillus niger를 단일 원인균으로 하는 병해로 인식되어 왔으나, A. welwitschiae, A. awamori 등 다수의 black aspergilli (Aspergillus section Nigri) 종들이 관여하는 복합병임이 보고되고 있다[13]. 이러한 연구 결과들은 양파 저장 병해를 단일 병원균의 단순한 감염 현상으로 이해하기보다는 전체 미생물 군집(microbiome)의 구조적 변화와 기능적 상호작용의 관점에서 접근해야 함을 시사한다[4,14]. 또한 양파 구가 다양한 분류군에 속하는 다수의 병원성 곰팡이에 의해 복합적인 위협에 노출되어 있음은 곰팡이 군집 조성(composition)이 병 발생 양상과 저장 중 부패 진행에 직접적인 영향을 미칠 수 있음을 의미한다. 그럼에도 불구하고 양파 구에서 군집 수준(community-level)의 곰팡이 다양성을 체계적으로 분석한 연구는 여전히 제한적인 실정이다.
체계적인 구 선발·처리·저장 기술을 설계하기 위해서는 수확기 양파 구의 병원성 및 비병원성 곰팡이 종들이 공존하며, 이들 군집이 저장 중 부패 진행 및 다음 작기의 병 발생에 어떠한 역할을 수행하는지에 대한 기초적 이해가 선행되어야 한다. 따라서 본 연구에서는 수확기 양파 구의 곰팡이 다양성을 군집 수준에서 분석하고, 이를 통해 국내 양파 재배 환경에서의 병원성 곰팡이 관리 전략 개발에 활용 가능한 과학적 기반 자료를 제공하고자 한다.
양파 품종 별 병원성 곰팡이의 오염도를 조사하기 위해 2024년 6월부터 7월까지 농촌진흥청 국립원예특작과학원 파속채소연구센터에서 재배된 양파 시판품종 및 육성계통 12개 품종(황색, 백색, 적색 양파)의 양파 구를 수집하였다. 또한 지역별 곰팡이 오염도를 평가하기 위해 무안, 함양, 창녕지역 8개 포장에서 황색 양파 시료를 추가적으로 수집하였다. 모든 시료는 수확 후 약 1달간의 건조과정을 거친 후 수집하였다. 각 품종 및 지역 포장별로 수확 후 건조된 양파를 3구씩 수집하였다. 겉껍질을 제거 후 3mm × 3mm 크기로 작게 자르고, 2% NaOCl 용액으로 2분간 표면소독하고 멸균수로 2회 세척하여 물기를 제거하였다. 조각난 양파는 스트렙토마이신(600 μg/mL)이 첨가된 potato dextrose agar (PDA; Difco, Detroit, MI, USA)와 dichloran-glycerol agar (DG18; Oxoid, Basingstoke, Hampshire, UK)에 100조각씩 치상하고 25℃ 항온기에서 5–7일 동안 배양하였다. 곰팡이 집락의 형태학적 특징을 이용하여 곰팡이를 PDA에 분리 배양하였다. 곰팡이의 발생빈도는 감염된 양파 조각의 수를 평가하여 백분율로 나타내었다.
분리된 곰팡이 균주는 DNeasy plant mini kit (Qiagen, Hilden, Germany)를 이용하여 genomic DNA를 추출하였다. 곰팡이 동정을 위해 internal transcribed spacer region (ITS)와 β-tubulin (BT) 유전자의 염기서열을 분석하였고, 각각 ITS1/ITS4 [15], Bt2a/Bt2b [16] primer set를 사용하였다. A. niger와 A. welwitschiae 등 Aspergillus section Nigri에 속하는 종들의 정확한 동정을 위해 calmodulin (CMD) 유전자를, Fusarium 속에 속하는 종들은 translation elongation factor 1-α (TEF-1 α)와 RNA polymerase II (RPB2)를 추가 분석하였다. 각 primer set는 cmd5/cmd6 [17], ef1/ef2 [18], fRPB2-7cF/fRPB2-11aR [19]을 사용하였다. 각각의 유전자로부터 얻은 염기서열은 DNASTAR (Lasergene 15, Madison, WI, USA)를 이용하여 교정 후, NCBI Genbank database를 이용한 BLAST 분석을 수행하였다.
Fusarium 속의 분리균주들은 TEF-1α 와 RPB2 유전자의 염기서열을, Aspergillus section Nigri에 속하는 균주들은 ITS와 CMD 유전자의 염기서열을 합하여 계통수를 작성하였다. 각 속의 염기서열들은 CLUSTAL X를 사용하여 정렬하고, 유사도 분석을 통해 대표 서열을 선발하였다. 각 속의 대표 염기서열은 근연관계의 염기서열과 함께 MEGA 12[20] 프로그램을 이용하여 maximumlikelihood 계통수를 작성하였다.
양파 구에서 분리된 Fusarium속 균주 6종(F. proliferatum, F. oxysporum, F. commune, F. acuminatum, F. fujikuroi, F. solani)에 대해 양파의 품종과 채집 지역 등을 고려해 18개 균주를 선발하여 병원성을 검정하였다. 선발된 균주들은 PDA 배지에 5일동안 배양 후, 증류수를 도포하고 셀 스크래퍼를 이용하여 배양체를 회수하였다. 이후 멸균된 miracloth로 균사 제거 후 포자농도가 1 × 105 spores/ mL이 되도록 현탁하였다. 양파(품종: 카타마루) 종자는 포자현탁액에 1시간동안 침지한 후 30립씩 파종하여 25℃, 습도 70%, 12시간 광조건/12시간 암조건 하에서 2주간 발병을 유도한 후 유묘의 생존률 평가를 통해 병원성을 검정하였다. 대조구는 멸균수에 침지하였으며, 실험은 3회반복 수행하였다.
수확 후 양파의 곰팡이 오염도를 조사하기 위해 품종 및 지역별로 총 20개 포장에서 양파를 수집하였다. 수집된 모든 양파에서 13–100% (66.5 ± 34.2%)의 곰팡이 오염도가 조사되었다(Fig. 1). 양파에서 가장 높은 오염도를 나타내는 곰팡이는 Aspergillus속(49.5 ± 36.3%) 이었으며, Fusarium속(27.2 ± 27.4), Penicillium속(4.9 ± 4.4%) 순이었다. 구피색에 따른 품종별 곰팡이 오염도를 조사하기 위해 무안 파속채소연구센터에서 재배된 12품종(황색 6품종, 자색 3품종, 백색 3품종)을 수집 분석한 결과, 총 곰팡이 오염도는 황색 양파의 경우 22–100% (80.3 ± 28.2%), 자색 90–100% (96.7 ± 4.7%), 백색 66–100% (88.7 ± 16.0%)로 조사되었다(Table 1). 양파 구피색에 따른 총 곰팡이 오염도는 자색 양파가 가장 높았다. 그러나, 가장 높은 오염도를 나타내는 곰팡이 분류군의 종류는 양파 구피색별로 차이를 보였다. 황색과 자색 양파의 경우 Aspergillus속 곰팡이가 각각 67.1 ± 40.0%와 81.3 ± 19.8%로 가장 높은 오염도를 나타내었으나, 백색 양파의 경우 Fusarium속 곰팡이가 64.4 ± 10.3%로 가장 높은 오염도를 나타내었다. 또한 황색 양파의 경우 Penicillium 속 곰팡이가 3.8 ± 4.1%의 오염도로 나타났으나, 자색과 백색 양파에서는 관찰되지 않았다.
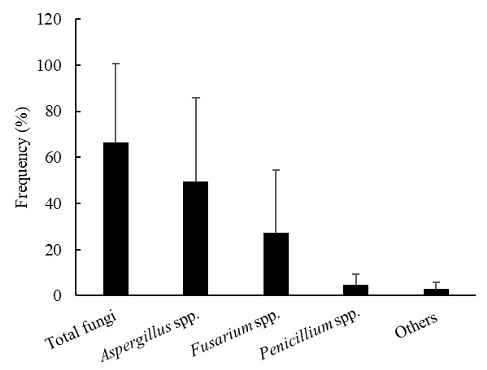
Fig. 1. Occurrence of fungi in onion bulb samples.
Table 1. Occurrence of fungi according to the color of onion bulbs
테일블
*The numbers in parentheses indicate the number of onion cultivars collected for each bulb color.
시판 품종 4종에 대한 곰팡이 오염도를 조사한 결과, 총 곰팡이 오염도는 카타마루가 가장 높게 나타났으며, 이어서 엄지나라, 맵시황, 화이트원 순으로 나타났다(Fig. 2). 카타마루에서는 Aspergillus속 곰팡이가 가장 우점하는 것으로 나타났으나, 화이트원, 맵시황에서는 Fusarium속 곰팡이가 가장 우점하는것으로 나타났다. 엄지나라의 경우는 Aspergillus속 및 Fusarium속 곰팡이가 비슷한 비율로 관찰되었다. 지역별 양파의 곰팡이 오염도를 조사한 결과, Aspergillus속 곰팡이가 가장 우점하는 것으로 나타났으며, 일부 지역시료에서만 Fusarium속 곰팡이가 4–17%의 오염도를 나타내었다(Fig. 3).
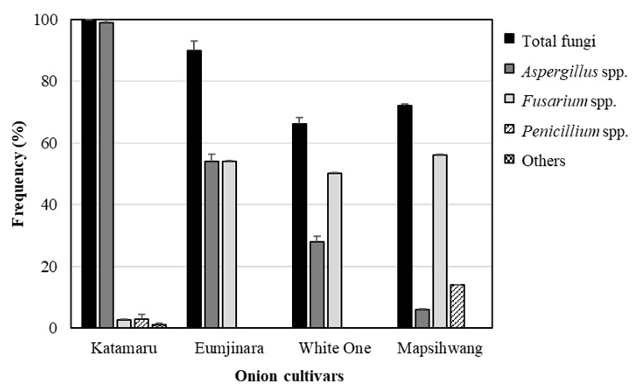
Fig. 2. Occurrence of fungi according to the onion cultivar.
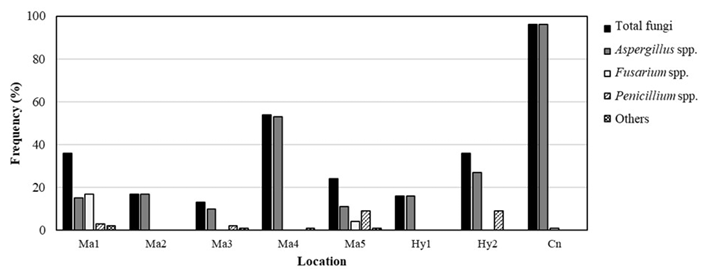
Fig. 3. Occurrence of fungi according to the cultivation region of onion. Ma, Muan; Hy, Hamyang; Cn, Changnyeong.
양파 시료에서 총 174개의 균주를 분리하였고, 곰팡이 오염도 조사결과와 같이 Aspergillus, Fusarium, Penicillium속 순의 빈도로 검출되었고, 자세히는, A. welwitschiae (42.0%), F. proliferatum (24.7%), P. brasilianum (6.3%), P. glabrum (5.2%) F. oxysporum (4.6%) 순의 빈도로 분리되었다(Table 2). 양파에서 분리된 Aspergillus속 곰팡이의 94.8%가 A. welwitschiae로 동정되었으며, A. montevidensis, A. sydowii등이 분리되었다. Fusarium속 곰팡이 중에서, F. proliferatum이 72.9%로 가장 많이 분리되었으며, F. oxysporum, F. commune, F. acuminatum, F. fujikuroi, F. solani 등이 분리되었다. Penicillium 속에서는 P. brasilianum, P. glabrum이 각각 42.3%와 34.6%로 가장 많이 분리되었고, P. brevicompactum, P. citrinum, P. ochrochloron 등이 분리되었다. 그 외에 Alternaria, Talaromyces, Chaetomium, Cladosporium, Coprinellus, Bipolaris, Circinella, Irpex, Phaeosphaeria, Curvularia 등이 분리되었다.
Table 2. Number of fungal isolates from onion bulbs
table
*The numbers in parentheses indicate the frequency of occurrence within each genus.
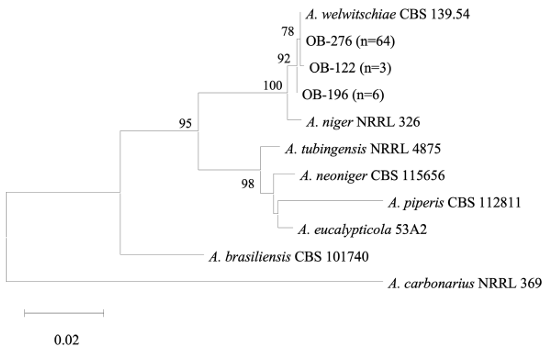
Fig. 4. A maximum likelihood tree derived from the combined sequences of the ITS and CMD genes of Aspergillus section Nigri isolates from onion bulbs. Bootstrap values (1,000 replicates) greater than 70% are shown next to branches.
양파에서 분리된 A. welwitschiae의 정확한 동정과 유전적 다양성을 평가하기 위해 ITS와 CMD 유전자를 이용하여 계통수 분석을 수행하였다. 73개의 A. welwitschiae균주는 종 내에서 3개의 유전적 그룹을 형성하였고, 기존에 보고된 A. welwitschiae CBS 139.54와 100% 유사성을 가지는 균주들이 87.7% (n = 64)로 가장 많이 분리되었다(Fig. 4). A. welwitschiae의 ITS region 염기서열은 A. niger의 염기서열과도 100%의 유사도를 가지기 때문에, 두 종간의 정확한 동정을 위해서는 CMD 유전자의 염기서열간 유사도를 비교하였다. A. welwitschiae 종 내에서 유전적 차이는 CMD 유전자 염기서열 차이이며, 균주들간 99.9%의 유사도를 나타내었다. Fusarium속 균주들은 TEF-1α 와 RPB2 유전자를 이용하여 계통수 분석결과 6개 Fusarium 종 내에서 유전적 그룹을 형성하였다(Fig. 5). 특히, 양파에서 시들음병을 일으키는 것으로 알려진 F. oxysporum은 종 내에서 3개의 유전적 그룹을 형성하였고, 가장 많이 분리된 F. proliferatum도 3개의 그룹을 형성하였다. 두 Fusarium 종 모두 종 내에서 99.2–100%의 염기서열 유사도를 나타내었다. Penicillium속 균주들은 ITS 와 BT 유전자를 이용한 계통수에서 5개 Penicillium 종 내에서 유전적 그룹을 형성하였다(Fig. 6).
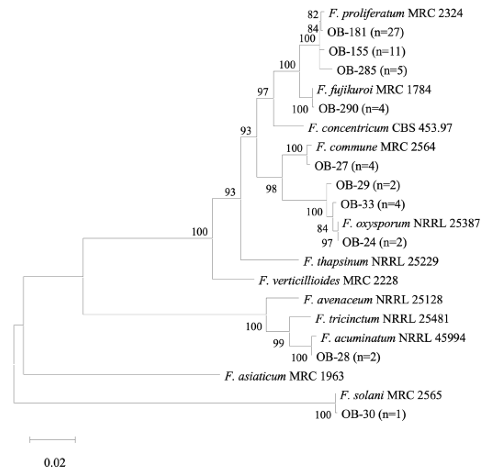
Fig. 5. A maximum likelihood tree derived from the combined sequences of the TEF-1α and RPB2 genes of Fusarium isolates from onion bulbs. Bootstrap values (1,000 replicates) greater than 70% are shown next to branches.
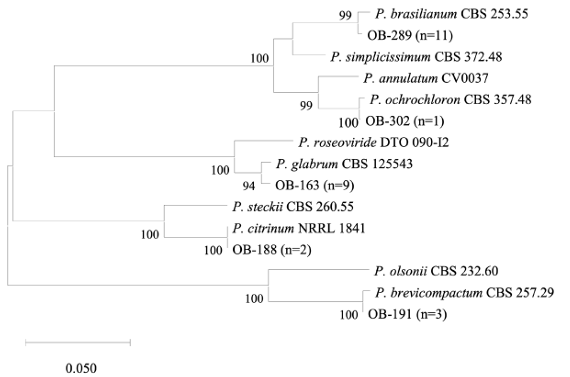
Fig. 6. A maximum likelihood tree derived from the combined sequences of the ITS and BT genes of Penicillium isolates from onion bulbs. Bootstrap values (1,000 replicates) greater than 70% are shown next to branches.
양파에서 분리된 Fusarium속 곰팡이 6종의 유묘기 양파에 대한 병원성을 검정하였다(Table 3). 병원성 검정결과 6종의 Fusarium 중 F. proliferatum에서 가장 강한 병원성이 나타났다. F. proliferatum은 9 균주 중 3 균주에서 63.5–87.4%의 발병율을 나타내었다. 특히 F. proliferatum OB124와 OB-141은 양파 종자에서 70% 이상의 미발아율을 나타내어 강한 병원성을 가지는 것으로 나타났다. 이 두 균주는 각각 카타마루와 엄지나라에서 분리되었다. F. oxysporum은 3개 중 1개 균주 에서만 13.8%의 발병율을 나타내었고, F. acuminatum은 18.4%의 발병율을 나타내었다. F. commune과 F. fujikuroi는 병원성이 확인되지 않았다.
Table 3. Pathogenicity of Fusarium species isolated from onion bulbs
table
ND: not detected.
2024년 국내에서 재배된 양파의 수확 후, 저장 전 단계에서 곰팡이 오염도 및 다양성을 평가하였다. 모든 시료에서 Aspergillus속과 Fusarium속 곰팡이가 관찰되었으며, A. welwitschiae과 F. proliferatum이 가장 많이 분리되었다. 이는 저장 유통단계의 부패 구를 대상으로 하거나, 특정 병원균(F. oxysporum, B. aclada, A. niger)에 집중되어 있는 기존의 연구 결과들과 다소 차이를 보였다. Silva 등은 [13] 브라질의 양파 생산부터 유통 체계를 대상으로 포장(field), 유통(market) 단계에서 black aspergilli 군집의 변화를 추적하였다. 포장단계에서는 Penicillium속 곰팡이가 우점하는 반면, 유통단계에서는 Aspergillus section Nigri, 특히 A. welwitschiae가 가장 빈번한 종으로 보고하였다. 국내 유통단계 양파에서도 Aspergillus (63.9%), Penicillium (15.5%), Fusarium (6.4%), Rhizopus (5.2%) 순으로 가장 많이 관찰되었으나, 주요 병원균으로는 A. awamori, F. oxysporum, P. brasilianum, R. oryzae 등을 보고하였다[21]. 이집트의 부패 저장구에서는 모든 시료에서 A. niger가 검출되었다[7].
수확 후 양파 구에서 우점하는 곰팡이 분류군은 재배 지역 및 품종에 따라 뚜렷한 차이를 나타내는 것으로 확인되었다. 본 연구에서 대부분의 황색 및 적색 양파에서는 A. welwitschiae가 우점종으로 관찰된 반면, 백색 양파에서는 F. proliferatum이 우점하는 것으로 나타났다. Penicillium속 곰팡이는 황색 양파에서만 관찰되었다. 다만, 황색 및 적색 양파의 각 1개 품종(엄지나라, 맵시황)은 동일한 구피색 양파의 군집 구조와 달리 F. proliferatum이 우점하였다. 이는 동일 환경하에서도 품종 또는 기주 유전형에 따라 내생·근권 미생물 군집은 뚜렷이 구분됨을 나타내며, 이러한 품종 특이적 군집 구조(cultivar-specific community structure)는 여러 작물에서 반복적으로 보고되어 왔다[22,23]. Kalman 등은[12] 부패 양파 구 연구에서, 동일 지역·품종 내에서도 곰팡이 종 수준에서의 계통 분화(clade)가 존재하고, 품종(자색 vs 백색) 및 지역(북부 vs 남부)에 따라 군집 구조가 유의미하게 달라짐을 보고한 바 있다.
본 연구에서 양파로부터 반복적으로 분리된 Fusarium속 곰팡이의 주요 종은 F. proliferatum (73%), F. oxysporum (13.6%), F. commune (6.8%)이었으며, 양파 종자에 대한 병원성은 F. proliferatum이 가장 높은 것으로 확인되었다. 이러한 결과는 선행연구들과도 일치하는 경향을 보였다. 최근 연구에서 수확 후 저장 단계의 양파 구에서 다양한 Fusarium fujikuroi species complex (FFSC) 구성원들(F. annulatum, F. thapsinum, F. fujikuroi)과, F. redolens, F. commune, F. solani 등이 검출되었으며, 특히 F. proliferatum이 98%의 비율로 단독 우점하는 군집 구조가 관찰되었다[24,25]. 또한 F. oxysporum과 F. proliferatum의 높은 양파 병원성은 다수의 연구를 통해 입증되었으며, 그 외에도 F. culmorum, F. redolens, F. acutatum, F. anthophilium, F. annulatum and F. acuminatum, F. solani, F. verticillioides 등 다양한 Fusarium 종들의 병원성이 보고되고 있다[12,26–29]. 그러나 Fusarium 분리균의 양파에 대한 병원성은 감염 대상 조직에 따라 병원성이 상이하게 관찰되었다. 일부 연구에서는 Fusarium 균주가 양파 구에 비해 종자에서 더 완만한 병징 발현을 보이며, 구에서 상대적으로 낮은 병원성을 나타낸다고 보고하였다[24]. 그러나 다른 연구들에서는 종자와 구에서 유사한 수준의 병원성을 보이거나, 양파의 생육단계에 따라 병원성 수준이 크게 달라지는 상반된 결과도 보고되었다[27,29–31]. 이러한 결과는 Fusarium 균주의 계통 및 병원형(pathotype) 차이, 양파 품종의 유전적 배경, 병원성 검정 방법론의 차이에 기인하는 것으로 추정된다.
수확 후 양파 곰팡이 오염도를 조사한 결과, 품종별, 재배 지역별로 관찰되는 곰팡이 분류군의 종류와 발생빈도가 다른 것으로 조사되었다. 이는 양파 구의 곰팡이 군집 구조가 생산, 수확, 저장 등 공급망 단계별 환경 변화에 대응하여 동적으로 재편될 수 있음을 보여주며, 단일 시점에서 수행된 조사만으로는 저장 병해의 발생 양상과 역학을 충분히 설명하기 어렵다는 점을 시사한다. 특히, 저장 병해를 소수의 특정 병원균에 기반하여 관리해 온 기존의 병해 관리 접근법은 중요한 한계를 지니는 것으로 판단된다. 따라서 양파의 저장 병해를 효과적으로 관리하기 위해서는 병원성의 종 다양성, 우점 구조, 그리고 이들에 영향을 미치는 지역적 및 품종 특이적 요인을 통합적으로 이해하는 것이 중요하다. 본 연구에서 도출된 결과는 향후 지역·품종 특성을 고려한 저장성 관리 전략 및 병해 예측 기반 구축에 중요한 근거 자료로 활용될 수 있을 것으로 기대된다.
본 연구에서는 양파(Allium cepa L.) 구(bulb)에서 발생하는 곰팡이 병원균의 발생현황을 규명하고, 형태학적·분자생물학적 분석을 통해 주요 병원성 곰팡이 종을 동정하였다. 전라남도 무안, 경상남도 함양 및 창녕 지역의 양파 재배지 및 저장고에서 양파 구를 수집하여 곰팡이 오염 실태를 조사한 결과, 양파의 곰팡이 군집은 주로 Aspergillus 속(49.5 ± 36.3%)가 우점하였으며, 그 다음으로 Fusarium 속(27.2 ± 27.4%)과 Penicillium 속(4.9 ± 4.4%)이 높은 비율로 검출되었다. 품종(구피색)에 따른 오염 양상의 차이가 뚜렷하게 나타나, 적색 및 황색 양파는 주로 Aspergillus spp. (6.0100%)에 의해, 백색 양파는 Fusarium spp. (50.0–73.3%)에 의해 더 높은 오염도를 보였다. 총 174개의 곰팡이 균주가 분리되었으며, A. welwitschiae (42.0%)가 가장 높은 빈도로 검출되었고, 다음으로 F. proliferatum (24.8%), P. brasilianum (6.3%), P. glabrum (5.2%), F. oxysporum (4.6%), F. commune (2.3%), A. montevidensis, P. brevicompactum 등이 확인되었다. Aspergillus속의 분리균의 94.8%가 A. welwitschiae로, Fusarium 속에서는 72.9%가 F. proliferatum으로 동정되었다. 이 밖에도 Bipolaris, Chaetomium, Circinella, Cladosporium, Coprinellus, Curvularia, Talaromyces 등도 확인되었다. 본 연구 결과는 재배 및 저장 과정에서 양파에 피해를 주는 주요 병원성 곰팡이로부터 보호하기 위한 방제 전략을 개발하는데 유용한 기초 자료로 활용될 수 있다. 다만, 보다 다양한 품종을 대상으로 하는 추가 연구가 필요하다.
No potential conflict of interest relevant to this article was reported.
This work was carried out with the support of “Cooperative Research Program for Agriculture Science and Technology Development (Project No. PJ01512801)” Rural Development Administration (RDA), Republic of Korea. And this study was supported by 2024 the RDA Fellowship Program of Allium Vegetable Research Center, Rural Development Administration, Republic of Korea.
1. FAOSTAT. Crops and livestock products: Production quantities of onions and shallots, green by country (Average 2019 – 2023) [Internet]. Rome: Food and Agriculture Organization of the United Nations; 2023 [updated 2025 Jun 11; cited 2025 Nov 26]. Available from: https://www.fao.org/
2. KOSIS. Crop production survey: Vegetable production (spice & culinary vegetables) [Internet]. Daejeon: Korean Statistical Information Service; 2025 [updated 2025 Nov 21; cited 2025 Nov 26]. Available from: https://kosis.kr/
3. Ji SH, Kim TK, Keum YS, Chun SC. The major postharvest disease of onion and its control with thymol fumigation during low-temperature storage. Mycobiology 2018;46:242-53. https://doi.org/10.1080/12298093.2018.1505245
[DOI]
4. Yurgel SN, Abbey L, Loomer N, Gillis-Madden R, Mammoliti M. Microbial communities associated with storage onion. Phytobiomes J 2018;2:35-41. https://doi.org/10.1094/PBIOMES-12-17-0052-R
[DOI]
5. Kiran PR, Aradwad P, Arun Kumar TV, Nayana NP, Ramya CS, Sahoo M, Urhe SB, Yadav R, Kar A, Mani I. A comprehensive review on recent advances in postharvest treatment, storage, and quality evaluation of onion (Allium cepa): Current status, and challenges. Future Postharvest Food 2024;1:124-57. https://doi.org/10.1002/fpf2.12009
[DOI]
6. Belo TR, du Toit LJ, Waters TD, Derie ML, Schacht B, LaHue GT. Reducing the risk of onion bacterial diseases through managing irrigation frequency and final irrigation timing. Agric Water Manag 2023;288:108476. https://doi.org/10.1016/j.agwat.2023.108476
[DOI]
7. El-Dawy EGAM, Hussein MA, El-Nahas S. Description and management of Aspergillus section Nigri causing post-harvest bulbs rot of onion. Sci Rep 2024;14:6076. https://doi.org/10.1038/s41598-024-53849-9
[DOI]
8. Kumar V, Neeraj SS, Sagar NA. Post harvest management of fungal diseases in onion-a review. Int J Curr Microbiol Appl Sci 2015;4:737-52.
9. Suravi TI, Hasan MK, Jahan I, Shopan J, Saha M, Debnath B, Ahammed GJ. An update on post-harvest losses of onion and employed strategies for remedy. Sci Hortic 2024;338:113794. https://doi.org/10.1016/j.scienta.2024.113794
[DOI]
10. Haapalainen M, Kuivainen E, Iivonen S, Niemi M, Latvala S. Pathogenicity of Fusarium oxysporum and Fusarium proliferatum isolates from symptomless onions (Allium cepa) and onions with Fusarium basal rot. Plant Pathol 2023;72:1122-35. https://doi.org/10.1111/ppa.13718
[DOI]
11. Shin JH, Lee HK, Back CG, Kang SH, Han JW, Lee SC, Han YK. Identification of Fusarium basal rot pathogens of onion and evaluation of fungicides against the pathogens. Mycobiology 2023;51:264-72. https://doi.org/10.1080/12298093.2023.2243759
[DOI]
12. Kalman B, Abraham D, Graph S, Perl-Treves R, Meller Harel Y, Degani O. Isolation and identification of Fusarium spp., the causal agents of onion (Allium cepa) basal rot in Northeastern Israel. Biology 2020;9:69. https://doi.org/10.3390/biology9040069
[DOI]
13. Silva JJ, Bertoldo R, Fungaro MHP, Massi FP, Taniwaki MH, Sant’Ana AS, Iamanaka BT. Black aspergilli in Brazilian onions: From field to market. Int J Food Microbiol 2021;337:108958. https://doi.org/10.1016/j.ijfoodmicro.2020.108958
[DOI]
14. Huang K, Sun X, Li X, Huang X, Sun Z, Li W, Wang J, Tian D, Lin C, Wu X, et al. Pathogenic fungi shape the fungal community, network complexity, and pathogenesis in kiwifruit. Microb Biotechnol 2023;16:2264-77. https://doi.org/10.1111/1751-7915.14344
[DOI]
15. White TJ, Bruns T, Lee S, Taylor J. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. In: Innis MA, Gelfand DH, Sninsky JJ, White TJ, editors. PCR protocols: A guide to methods and applications. Vol. 18. New York: Academic press; 1990. p. 315-22.
[DOI]
16. Glass NL, Donaldson GC. Development of primer sets designed for use with the PCR to amplify conserved genes from filamentous ascomycetes. Appl Environ Microbiol 1995;61:1323-30. https://doi.org/10.1128/aem.61.4.1323-1330.1995
[DOI]
17. Hong SB, Cho HS, Shin HD, Frisvad JC, Samson RA. Novel Neosartorya species isolated from soil in Korea. Int J Syst Evol Microbiol 2006;56:477-86. https://doi.org/10.1099/ijs.0.63980-0
[DOI]
18. O’Donnell K, Kistler HC, Cigelnik E, Ploetz RC. Multiple evolutionary origins of the fungus causing Panama disease of banana: Concordant evidence from nuclear and mitochondrial gene genealogies. Proc Natl Acad Sci 1998;95:2044-9. https://doi.org/10.1073/pnas.95.5.2044
[DOI]
19. Liu YJ, Whelen S, Hall BD. Phylogenetic relationships among ascomycetes: Evidence from an RNA polymerase II subunit. Mol Biol Evol 1999;16:1799-808. https://doi.org/10.1093/oxfordjournals.molbev.a026092
[DOI]
20. Kumar S, Stecher G, Suleski M, Sanderford M, Sharma S, Tamura K. MEGA12: Molecular evolutionary genetic analysis version 12 for adaptive and green computing. Mol Biol Evol 2024;41:msae263. https://doi.org/10.1093/molbev/msae263
[DOI]
21. Oh JY. Identification of predominant fungi isolated from market onion and antifungal activity of thymol against pathogenic fungi on stored onions in Korea [dissertation]. Seoul: Korea University; 2018.
22. Manter DK, Delgado JA, Holm DG, Stong RA. Pyrosequencing reveals a highly diverse and cultivar-specific bacterial endophyte community in potato roots. Microb Ecol 2010;60:157-66. https://doi.org/10.1007/s00248-010-9658-x
[DOI]
23. Castanera R, González-Miguel VM, Escolà G, Olivé M, Teixidó N, Savé R, Casacuberta JM, San Segundo B. Cultivar-dependent variations in the microbiome of grapevine leaves. Horticulturae 2024;10:1333. https://doi.org/10.3390/horticulturae10121333
[DOI]
24. Diabankana RGC, Frolov M, Islamov B, Shulga E, Filimonova MN, Afordoanyi DM, Validov S. Identification and aggressiveness of Fusarium species associated with onion bulb (Allium cepa L.) during storage. J Fungi 2024;10:161. https://doi.org/10.3390/jof10020161
[DOI]
25. Ghanbarzadeh B, Mohammadi Goltapeh E, Safaie N. Identification of Fusarium species causing basal rot of onion in East Azarbaijan province, Iran and evaluation of their virulence on onion bulbs and seedlings. Arch Phytopathol Plant Protect 2014;47:1050-62. https://doi.org/10.1080/03235408.2013.829628
[DOI]
26. Vetrova S, Alyokhina K, Engalycheva I, Kozar E, Mukhina K, Sletova M, Krivenkov L, Tikhonova T, Kameneva A, Frolova S, et al. Identification and pathogenicity of Fusarium species associated with onion basal rot in the Moscow Region of Russian Federation. J Fungi 2024;10:331. https://doi.org/10.3390/jof10050331
[DOI]
27. Le D, Audenaert K, Haesaert G. Fusarium basal rot: Profile of an increasingly important disease in Allium spp. Trop Plant Pathol 2021;46:241-53. https://doi.org/10.1007/s40858-021-00421-9
[DOI]
28. Shin JH, Lee HK, Lee SC, Han YK. Biological control of Fusarium oxysporum, the causal agent of Fusarium basal rot in onion by Bacillus spp. Plant Pathol J 2023;39:600-13. https://doi.org/10.5423/PPJ.OA.08.2023.0118
[DOI]
29. Dutta R, Jayalakshmi K, Kumar S, Radhakrishna A, Mahajan V. Standardization of challenge inoculation protocols for artificial infection of Fusarium acutatum and Fusarium falciforme causing basal rot of onion. Sci Rep 2025;15:39648. https://doi.org/10.1038/s41598-025-23382-4
[DOI]
30. Le D, Ameye M, De Boevre M, De Saeger S, Audenaert K, Haesaert G. Population, virulence, and mycotoxin profile of Fusarium spp. associated with basal rot of Allium spp. in Vietnam. Plant Dis 2021;105:1942-50. https://doi.org/10.1094/PDIS-08-20-1850-RE
[DOI]
31. Taylor A, Vágány V, Jackson AC, Harrison RJ, Rainoni A, Clarkson JP. Identification of pathogenicity-related genes in Fusarium oxysporum f. sp. cepae. Mol Plant Pathol 2016;17:1032-47. https://doi.org/10.1111/mpp.12346
[DOI]