Department of Microbiology, Dankook University, Cheonan 31116, Korea
*Correspondence to piceae@dankook.ac.kr
Korean Journal of Mycology (Kor J Mycol) 2025 December, Volume 53, Issue 4, pages 237-243.
https://doi.org/10.4489/kjm.2025.53.4.1
Received on October 17, 2025, Revised on November 10, 2025, Accepted on November 10, 2025, Published on December 31, 2025.
Copyright © The Korean Society of Mycology.
This is an Open Access article which is freely available under the Creative Commons Attribution-Non-Commercial 4.0 International License (CC BY-NC) (https://creativecommons.org/licenses/by-nc/4.0/).
Fungal taxonomy provides a fundamental framework for understanding the biodiversity, ecology, medical relevance, and industrial applications of fungi. In recent years, on the basis of development in high-resolution phylogenomic and molecular systematic studies, the classification of fungi has undergone considerable advances. Contrastingly, in Korea, the traditional 4–7 phylum model still prevails, although fails to adequately reflect recent trends. In this review, we summarize advances over the past decade in the study of Mucoromycota, Zoopagomycota, Entorrhizomycota, and Aphelidiomycota. In addition, we describe the 19-phyla, 9-subkingdom classification system now registered in international databases, such as MycoBank and Index Fungorum. Finally, we highlight the need to adopt an updated classification system in Korean academia, education, biodiversity research, and pathogen diagnostics, and outline practical strategies and a roadmap for its implementation.
19-phyla, Fungal taxonomy, High-level classification, Phylogenomics
균류(fungi)는 극한 환경을 포함한 다양한 생태계에 분포한다[1]. 균류의 분류는 균류의 생물다양성, 생태, 의학 및 산업적 중요성을 이해하는 데 중요한 기반을 제공한다[2,3]. 잘 마련된 분류 체계는 균류의 다양한 특성을 파악하고 활용을 증진하기 위해 필요하며, 균류의 진화적 관계를 명확히 하고, 새로운 종 및 계통군의 발견과 동정을 가능하게 한다[4,5]. 역사적으로 균류 분류는 형태학 특징과 포자 형성과 관련된 균체의 구조 방식에 따라 Ascomycota, Basidiomycota, Zygomycota와 같은 광범위한 문으로 발전하였다[6,7]. 그러나 형태학 특징은 진화적 관계를 충분히 반영하지 못하였다[8].
분자계통학에 있어서, 특히 보존된 단백질을 암호화하는 유전자와 리보솜 마커 염기서열을 사용하는 다유전자좌위 계통분석 및 계통유전체학(phylogenomics) 방법의 출현은 균류 분류학 획기적인 변화를 불러왔다[9,10]. 이러한 방법들은 형태만으로는 접근하기 어려운 복잡한 진화적 관계를 밝혀내어 다계통군을 드러내고 숨겨진 다양성을 밝혔다[11]. 특히, 분자적 분석 자료는 Zygomycota가 다른 mycota와 관련 없는 계통으로 구성되어 있음을 지속적으로 지적하였고, 급기야 Zygomycota는 해체되었고 Mucoromycota, Zoopagomycota 등을 포함한 여러 별개의 문(phylum)이 새로 형성되었다[12,13]. 지속된 연구에서 유전체 기반의 고해상도 계통수 분석을 통해 균류 계(The Kingdom of fungi)는 최소 18개의 독립된 문(phylum)과 9개의 아계(subkingdom)로 분류하는 새로운 분류 체계가 제안되었다[14,15]. 이후 2024년 1개의 문이 추가되어 19문이 정식으로 인정되었다[16]. 이러한 동향에서 나타난 균류 분류의 새로운 틀은 형태적 유사성에 의존하던 고전적 분류 방식에서 벗어나, 진화 계통에 기반한 분류학적 기준을 제공하고 있다[17]. MycoBank (https://www.mycobank.org)나 Index Fungorum (http://www.indexfungorum.org) 등과 같은 국제 균류 데이터베이스에도 최근의 신규 분류 체계를 반영한 정보가 등록되었다.
이러한 국제적 균류 분류 체계 변화에도 불구하고, 국내의 경우에는 여전히 5–11문 체계에 기반한 이전 균류 분류 체계에 머물러 있고, 아직 개정된 체계를 잘 반영하지 않고 있는 실정이다. 그 결과 현재 국내 연구자들은 상이한 분류 체계를 사용하는 경우가 많고, 대학 교육과 의학과 수의학의 임상 현장 및 식물병리학 분야에서 4문 모델이 여전히 사용되고 있다. 균류는 방대하며 종 다양성이 강조된다[18]. 따라서 지식의 공백을 식별하고 협력을 적극적으로 추진해야 한다[19]. 본 총설은 이러한 국내외 분류 체계 간의 격차를 해소하고, 개선된 분류 체계의 국내 도입을 장려하며, 최신 계통유전체학적 증거를 바탕으로 한 균류 분류 체계 발전을 촉구하고자 작성되었다.
역사적으로 균류는 식물계(plantae)에 포함되거나 독립된 하나의 kingdom으로 간주되어 왔다[20]. 그러나 광합성 능력의 부재, 에너지 저장을 위해 글리코겐(glycogen)을 사용, 세포벽의 키틴(chitin) 구성, 무성과 유성생식 방식 보유, 진핵세포로 구성된 특성 등으로 인해 진균계(fungi kingdom)는 점차 식물과 구별되기 시작하였다[21,22].
20세기 중반까지는 주로 형태와 번식 구조에 기반하여 균류를 분류했다. 초기 분류 체계에서는 포자 형성 방식(예: 유성/무성), 균사에 격벽 존재 여부, 번식 기관의 형태 등이 주요 기준으로 사용되었다. 이러한 체계는 Ascomycota, Basidiomycota, Chytridiomycota, Zygomycota 등의 4문(phylum) 체계이다[23]. 2001년에 Glomeromycota가 추가된 후, 5문 체계가 가장 널리 사용되었다[24]. 대부분의 교육 자료와 연구에서 기본 분류 체계로 사용되었다. 그러나 Zygomycota 경우는 형태학적 유사성에 근거한 인위적 집합으로서 계통학적으로 다계통(paraphyletic)이라는 점이 계속해서 지적되었다. 분자계통학의 발전과 함께 rRNA 유전자(ribosomal RNA gene), 베타-튜불린 유전자(β-tubulin gene), RNA 중합효소 II 유전자(RNA Polymerase II largest/second largest subunit, RPB1/2), 신장 인자 1-알파 유전자(Elongation Factor 1-alpha, EF-1α) 등의 염기서열 정보가 계통 발생 연구를 위한 중요한 유전자 마커로 활용되면서, 기존 분류 체계의 문제점이 명확히 드러나, 결국 Zygomycota 분류군은 해체되었다. 이는 곧 균류 분류 체계가 더 이상 형태적 단순성에 의존할 수 없음을 보여주는 사례였으며, 유전체 기반 접근의 필요성을 크게 부각시켰다[8,25]. 이러한 계통학적 분류 체계 재편은 단순한 명칭 변경뿐만 아니라 균류의 병원성 기작, 생태적 기능, 공생방식에 대한 이해를 크게 증진시켰다. 예컨대, 인체에 기회감염을 유발하는 Mucorales는 Mucoromycota로 재분류되었으며, 현재 임상의학에서는 Zygomycosis 대신 Mucormycosis, Entomophthoramycosis로 개별 명칭을 명확히 구분해 사용하는 것이 정립되었다[26]. 또한, 형태가 유사하더라도 유전체의 크기, 유전자 군집의 배열(synteny), 생합성 경로의 존재 여부 등에서 현저히 다른 특징을 보이는 사례들이 발견되면서, 형태 기반 분류 체계의 한계가 보다 분명해졌다[27]. 결과적으로, 고전적인 균류 분류 체계는 더 이상 현대 균류학이 요구하는 정확한 종 동정을 충족시키기 어렵게 되었다, 이에 따라 유전체 기반의 통합적이고 계통학적으로 타당한 분류 체계로의 전환이 필요하다는 인식이 확산되었다[5].
분자계통학은 유전자 염기서열, 특히 리보솜 RNA(rRNA), β-tubulin, EF-1α 등의 유전 마커를 기반으로 한 계통수 분석을 통해, 형태학적 유사성과는 무관한 진화적 관계를 밝혀내는 도구로 자리 잡았다[28]. 초기에는 internal transcribed spacer (ITS) 영역이나 18S rDNA, 28S rDNA에 기반한 유전자 분석이 주로 활용되었지만, 유전자 분석 기술 발달에 따라 수십 개에서 수백 개의 유전자를 포함하는 유전체 기반 계통분석인 계통유전체학분석(phylogenomics)으로 전환되었다[29]. 계통유전체학(phylogenomics)은 단일 또는 소수 유전자가 나타내는 한계를 극복하고, 진화적 신호를 더 정교하게 해석할 수 있게 한다. 295개의 단백질 코딩 유전자를 기반으로 균류의 주요 분류군들을 고해상도로 해석한 결과는 Mucoromycota와 Zoopagomycota를 별개의 문으로 분리하는 데 핵심적인 근거를 제공하였다[13]. 계통유전체학의 발전은 단지 계통수 상의 위치를 밝히는 것에 그치지 않고, 병원성 요소, 생리적 특성, 생태적 적응 등의 진화적 함의를 탐색할 수 있게 이끌었다. Mucoromycota 계열 균류의 병원성 진화는 반복적인 유전자 손실과 획득, 수평적 유전자 이동을 통해 형성되었음을 보여주며, 이는 임상적으로 중요한 균류의 진단에도 기초 정보를 제공할 수 있다[30].
Zygomycota는 오랜 기간 동안 접합균문(Zygomycota)이라는 하나의 문으로 분류되어 왔으나, 분자계통학 및 유전체 분석의 발전으로 인해 이 분류군이 다계통성(polyphyly)을 갖는다는 사실이 명확히 밝혀졌다[11]. 이로 인해 Zygomycota는 해체되었으며, Mucoromycota (Mucoromycotina, Mortierellomycotina, Glomeromycotina), Zoopagomycota (Entomophthoromycotina, Kickellomycotina, Zoopagomycotina)로 재분류되었다[13].
Mucoromycota는 일반적으로 식물의 근권에 서식하거나 생물체를 부생적으로 분해하는 생태적 기능을 가진 균류들이 포함되며, 일부는 인간에게 치명적인 털곰팡이증(Mucormycosis)의 원인이 된다. 털곰팡이증은 주로 Mucorales 목(order)의 여러 종, 특히 Rhizopus, Mucor, Lichtheimia 속에 속한 종들에 의해 유발된다. 사람을 포함한 포유류에서 면역억제 상태에서 치명적인 침습성 감염을 일으킬 수 있다. 최근의 분자계통학 및 유전체 비교 연구들은 이러한 병원균의 진화적 경로를 규명하는 데 중요한 기여를 하고 있다[30]. 최근 유전체 기반 연구들은 병원성 Mucoromycota 계통에서 병원성 관련 유전자군의 반복적 획득, 유전자 중복, 유전체 재배열이 병원성 진화에 핵심적인 역할을 한다는 점을 밝혀내고 있다. 병원성 유전자군이 수렴진화 또는 유전자 중복을 통해 독립적으로 진화했음을 제시하였다[26]. 이러한 결과는 기존의 단순한 형태학 기반 분류 체계로는 설명하기 어려웠던 병원성 발현 메커니즘을 계통학적 관점에서 조망할 수 있게 하였다. 철 이온을 획득하는 siderophore 생합성 유전자, 산화 스트레스 반응 관련 유전자, 온도 적응 결함 관련 유전자 계열의 진화적 변화 등이 병원성 진화에 핵심적인 역할을 하는 것으로 보고있다[31–34]. 이들 유전자는 환경 내 기회감염성 균류의 생태적 적응력을 높이며, 비병원성 종과 분자적으로 구분이 가능하게 한다. 또한, Mucorales 내에서의 수평적 유전자 전달의 흔적은 병원성 진화의 또 다른 경로를 시사하며, Mucoromycota 전체의 진화적 유연성과 병원성 진화의 복잡성을 반영한다[35]. 이러한 분석은 초기 균류의 기원을 밝히는 데 기여하는 동시에, 현대 의학에서 위협이 되는 병원성 균류의 진화적 배경과 생태 적응 전략을 이해하는 데 실질적인 기초 자료가 되고 있다.
Zoopagomycota는 주로 무척추동물이나 원생생물을 포식하거나 기생하는 형태를 가지며, 종종 생물학적 방제 생물체로 연구된다. 유전체 분석을 통해 철 획득 단백질 관련 유전자, 스트레스 반응 유전자, 그리고 병원성 관련 유전자 등이 이들 계통에서 반복적으로 진화했다는 사실이 밝혀졌다[30].
Entorrhizomycota는 오랫동안 Basidiomycota와 혼동되었던 속(Entorrhiza 등)을 분리하여 신설된 문으로, 식물 뿌리에 결절 또는 혹을 형성하는 기생균이다. 이전까지는 Basidiomycota의 하위 계통인 Ustilaginomycotina로 분류되었다. 그러나 리보솜 유전자 및 미세구조적 특성을 근거로 이들은 독립된 문으로 분리되었다. 동포자 유사 구조, 이핵 균사 유지, 유사한 번식 방법을 갖고 있다는 점에서 Basidiomycota와 공통점을 가지고 있지만 유연공격벽, 꺽쇠연결, 담자기 형성이 없다는 점에서 구별된다. Entorrhiza 속은 기존의 Basidiomycota와 다른 독립적인 진화의 역사를 가지며, Basidiomycota와 Ascomycota의 공통 조상보다 더 이른 시점에 분기한 것으로 추정된다[36].
Aphelidiomycota는 조류(algae)에 기생하는 단세포성 균류로, 숙주 세포 내부로 침입하여 영양을 흡수하는 포식성 생활사가 특징이다. 유주자는 숙주 세포벽을 관통하여 아메바형 영양체(amoeboid trophont)로 전환되며, 숙주의 세포질을 직접 포식하고 소화한 뒤 다수의 유주자를 방출하는 유주자낭을 형성한다. 이러한 영양 방식은 진정한 균류의 흡수영양과 뚜렷하게 구별되며, Holomycota 내에서 독자적인 계통으로 자리매김하였다. 이전에는 Cryptomycota와 함께 취급되었으나, 초미세구조 및 rRNA 유전자 분석에 따라 독립된 문으로 격상되었다[37].
Cryptomycota는 Rozellomycota로도 알려져 있으며, 대부분 편모를 지닌 포자를 가지며 기생적 생존 양식을 보인다. 이들은 다양한 숙주(균류, 조류 등)에 기생하며, 핵심 염기서열의 부재 및 구조 유전자 손실로 인해 축소적 진화를 한 것으로 보인다[38]. Rozellomycota라는 명칭은 Cryptomycota와 동일하게 2011년에 제안되었으나, 명명 규약상 우선권을 확보하지 못하였다. 2011년 11월, 학술지 IMA Fungus에 Cryptomycota라는 명칭이 국제식물명명규약(ICN)의 모든 요건을 충족한 상태로 유효하게 출판되었다[38]. 그로부터 한 달 후인 12월, James & Berbee 등은 동일한 계통군에 대하여 Rozellomycota라는 명칭을 사용하였으나, 이는 출판 시점이 늦었다[39]. 국제식물명명규약(ICN, International Code of Nomenclature)에서의 규정은 유효 출판과 우선권(priority) 원칙에 기인한다. ICN에 따르면 동일한 계통군에 대해 복수의 명칭이 제안된 경우, 가장 먼저 유효하게 출판된 명칭이 정식 명칭으로 채택된다[40]. Rozellomycota는 분류학적 동의어로 처리되었다. 현재 MycoBank와 Index Fungorum 등 국제 공인 데이터베이스에서도 Cryptomycota는 공식 명칭으로 기재되어 있다. 다만, Rozellomycota는 대표 속명(Rozella)을 반영하고 곰팡이 문의 명명 관례(-mycota 접미)를 따르는 명칭이므로, 계통분류학 문헌에서는 여전히 병용되거나 선호되는 경향이 있다. 예를 들어, MycoBank에서 Rozella 속을 검색하면 분류 체계에는 Rozellomycota가 표시되지만, Rozellomycota의 현재 이름(current name)은 Cryptomycota로 명시되어 있다.
Sanchytriomycota는 Galindo 등(2021)에 의해 정의된 새로운 문으로, 주로 담수성 조류에 기생하는 원시적 기생 균류 그룹이다[16]. 이들은 단편적인 운동성을 가지지만, 유주자는 단일 후편모를 가지고 있으며, 그 편모의 구조는 진화적으로 크게 퇴화하여 기능이 상실되었고, 추진력은 매우 제한적이다. 따라서 이 편모는 실제로 비운동성인 ʻ의사편모(pseudocilium)’로 간주된다. 이들은 주로 담수성 조류에 기생하며, 운동성을 가지나 편모의 구조가 진화적으로 퇴화한 형태를 보인다. 이들은 숙주 세포벽에 부착 후, 숙주 세포질을 흡수하여 생활사를 완성한다. 또한 Sanchytriomycota의 편모 균류(flagellated fungi) 구조는 매우 특이한데, 편모의 기본기관인 기저체(kinetosome)는 길고 단순화된 형태를 띠는데, 이는 편모 구조가 점진적으로 축소되고 있음을 시사한다. Blastocladiomycota와 자매군 관계를 이루며, 독립적인 문으로서 빠른 진화 속도와 편모의 점진적 상실 과정을 보여주고 있다. 이 문은 Rozellomycota와 유사한 형태적 특징을 공유하나, 계통학적으로 뚜렷한 분기를 이루며 Holomycota의 매우 초기 단계의 그룹으로 제안되었다. 이처럼 Sanchytriomycota는 진화상에서 매우 오래전에 갈라져 나온, 독자적이고 원시적인 특징을 지닌 문으로 간주된다[16].
Aphelidiomycota, Cryptomycota, Sanchytriomycota 분류군들은 형태적으로는 명확한 균류의 특성을 보이지 않지만, 분자계통학적으로 진정한 균류의 일원으로 재정의되었으며, 진균계의 기원과 진화에 대한 이해를 심화시키는 데 중요한 기여를 하고 있다[14].
Tedersoo et al. (2018)은 진균계(Fungi)의 분류 체계를 기존의 4–6문(phylum) 체계에서 총 19문으로 확장하고, 이들을 9개의 아계(subkingdom)로 재정립하였다[14]. 이는 기존의 rDNA나 단일 유전자를 이용한 계통수보다 훨씬 높은 해상도를 제공하며, 고전 분류 체계의 오류를 교정하고 균류의 계통적 경계를 명확히 설정하는 데 기여하였다. 대표적으로 1,000개 이상의 균류 유전체와 환경 서열 데이터를 통합하여, 진균계를 18개의 문과 9개의 아계로 구분하였다[14]. 이후에 Sanchytriomycota가 문으로 인정이 되면서 19문 9아계가 되었다[40].
9개 아계는 주로 형태적 차이와 진화적 시기, 유전체 복잡성에 따라 정의되며, 대표적으로 Dikarya, Mucoromyceta, Chytridiomyceta, Zoopagomyceta, Blastocladiomyceta, Aphelidiomyceta, Rozellomyceta, Olpidiomyceta, Entorrhizomyceta 등이 포함된다[14]. 이러한 현대 분류 체계를 아계(subkingdom) 수준에서 정리하였다(Table 1)[14,16]. 문의 국명은 하위분류군에서 우리말 이름이 있은 것은 상위분류군에 그대로 인용하여 작성하였고 아직 이름이 없는 문은 라틴식 발음을 따라 명기하였다. 이는 이해를 돕기 위해 아직 편의상 작성된 것으로 아계와 아종을 포함해서 하위 분류군인 강 수준까지 한국균학회 균학용어심의위원회의 작업이 필요한 사항이다. 이전에 보고된 자료와 2023년도에 새로 추가된 강(Class)까지 포함하여 균류 계통수를 임의로 제시하였다(Fig. 1)[14,16,17,41–47].
이 분류 체계는 단순한 계통 정립을 넘어 생태적 해석, 병원성 예측, 대사 기능 비교 등 다양한 생물학적 질문에 대한 해석의 기반을 제공하고 있다[13]. 균류의 진화적 다양성과 고등 분류학적 단위를 보다 실질적으로 반영하고 있으며, MycoBank와 Index Fungorum 등 주요 데이터베이스에서도 채택되었다. 이러한 분류 체계는 단순히 이름의 변화가 아니라, 균류의 생태적 다양성과 진화적 기원을 명확히 이해하는 데 있어 핵심적인 틀을 제공한다. 각 문은 고유의 유전적, 형태학적, 생리학적 특성을 기반으로 정의되며, 향후 환경변화에 따른 진화 경로 예측 및 신종 탐색에도 중요한 기준점으로 활용될 수 있다.
Table 1. The list of subkingdom, phylum, and subphylum in the kingdom of Fungi recently registered in MycoBank and Index Fungorum
table
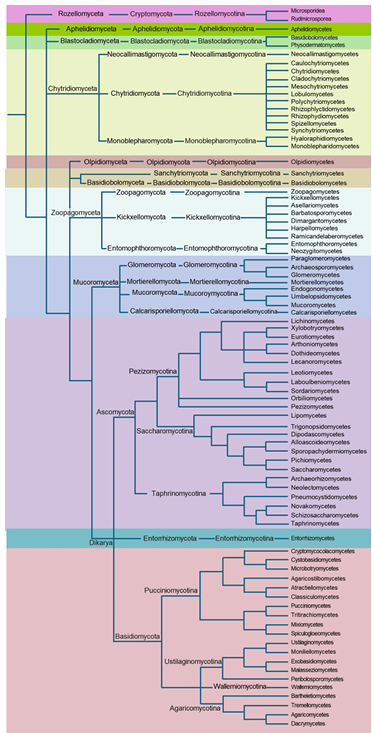
Fig. 1. Illustration of phylogram of fungal kingdom showing high-level classification including subkingdoms, phyla, and subphyla. The phylogram has been compiled based on several recent fungal taxonomic reports.
4.2.1. Dikarya
균계의 가장 대표적인 아계로, 전체 균류 종수의 98% 이상을 차지한다[48]. 생식 단계인 이핵 단계(dikaryotic stage)가 이름의 기원이다[49]. 이 단계는 세포 분열 후에도 두 개의 상이한 핵이 한 세포 내에 공존하는 것이 특징으로, 다른 균류와는 명확히 구별되는 점이다[8].
Ascomycota는 자낭과로 보호된 자낭 내에서 자낭포자를 형성하는 균문으로 정의되며, 분생포자인 무성포자도 생성한다[50,51]. 효모(Saccharomyces), 사상성 곰팡이(Aspergillus), 송로버섯(truffle) 등 다양한 종들이 포함되어 있다[51,52]. 다양성이 가장 큰 분류군이며 곰팡이 독소(mycotoxin)를 생성하는 종을 다수 포함하며, 산업적, 의학적, 식물병리학적으로 매우 중요하다[53–55].
Basidiomycota는 버섯, 녹병균, 깜부기병균을 포함하며 담자기에서 포자를 형성한다[56,57]. 목재 분해와 부생균[58,59], 농업[47], 임업[60,61], 의학[62,63], 식물병원균으로 중요한 분류군이다[64].
Entorrhizomycota는 과거 Basidiomycota (Ustilaginomycotina)에 속했으나 독립된 계통으로 분리되었다. 식물 뿌리 기생성 균류며, 규칙적인 격벽이 있는 나선형 균사를 가진다[36]. 단자엽 식물에 국한된 감염체로서 식물병리학분야에서 깜부기균으로 잘 알려진 분류군이다[43]. 대표적으로 옥수수 깜부기병균(Ustilago maydis)이 있다[65].
4.2.2. Mucoromyceta
전통적으로 Zygomycota에 포함되었던 균류가 유전체 분석을 통해 재편되어 형성된 아계. 주로 균근균, 뿌리 내생균, 식물 분해자로 구성된다[13].
Mucoromycota는 탄소가 풍부한 기질에서 빠르게 성장하는 초기 정착균으로, 여러 종이 산업계에서 유기산 생산 및 발효에 사용된다[66]. Mucormycosis는 Mucorales 목에 속하는 균류(Rhizopus, Mucor, Lichtheimia 등)에 의해 유발되는 균류증이다[67,68].
Mortierellomycota는 목본 식물의 뿌리에 사는 균근내생균(root endophytes)이자 부생균으로 흔히 분리되는 일반적인 토양 균류이다[69].
Glomeromycota는 식물 뿌리에 공생하는 arbuscular mycorrhizal fungi이다. 식물의 무기 영양분 흡수(특히 인산염)를 돕고, 식물 뿌리세포 내에 수지상체(arbuscule) 또는 소낭(vesicle)을 형성한다[24].
Calcarisporiellomycota는 드물게 보고된 계통으로, 토양에서 부생균으로 물질분해와 물질순환의 역할을 한다[70].
4.2.3. Zoopagomyceta
다양한 곰팡이 및 소형 동물(선충, 원생동물 등)에 기생 또는 공생하며, 주로 흡기 기생성 (haustorial parasitism) 혹은 융합형 기생을 보인다.
Zoopagomycota는 곰팡이 및 소형 동물에 기생하거나, 일부는 흙 속에서 사상균으로 생활한다[71]. Spatafora et al. (2016)[13]은 Zoopagomycota를 신설하면서 Entomophthoromycotina, Kickxellomycotina, Zoopagomycotina의 세 아문을 포함하는 분류 체계를 제안하였다. 이후 Tedersoo et al. (2018)은 이 중 Entomophthoromycotina와 Kickxellomycotina를 각각 독립적인 문으로 승격하였으며, 현재 Zoopagomycota에는 Zoopagomycotina만이 단일 아문으로 포함된다[14].
Entomophthoromycota는 주로 곤충(특히 파리목 등)에 기생하는 강력한 곤충병원성 균류로 구성되어 있다. 일부분은 토양 내 사상균으로도 생활한다. 동물 및 인간 감염 사례도 보고되었다[71]. Entomophthoromycosis 열대 및 아열대 지역에서 흔히 발생하는 드문 피하 및 점막 피부 균류 감염증이다[72].
Kickxellomycota는 절지동물의 내부(주로 내장)에서 공생하거나, 토양 및 분변 환경에서 생활하는 균류로 구성되며, 특이한 형태의 균사구조와 모발포자(trichospore) 등 특수한 무성생식 구조를 가진다[71,73].
4.2.4. Olpidiomyceta
Olpidiomycota는 Olpidiales를 포함하기 위해 신설되었다[74]. Olpidiales는 이전에 Chytridiomycetes 내 Spizellomycetales로 분류된 바 있다[75]. Olpidiomycota는 전 세계적으로 분포하며 식물, 조류, 윤충에 기생한다[76,77].
4.2.5. Basidiobolomyceta Basidiobolomycota는 토양, 곤충, 썩은 식물, 파충류와 양서류[78], 동물[79]의 장내에서 분리되며[80], 주로 Basidiobolus ranarum가 사람과 동물에 기회감염을 일으킨다[81,82]. 감염 증상은 피부 및 피하 조직 침범이 주를 이루며[83,84], 드물게 위장관 감염 및 전신 감염을 동반한다[85]. Basidiobolomycosis는 이러한 감염증을 의미하며, 위장관 감염(gastrointestinal basidiobolomycosis)은 주로 면역이 정상인 환자에게도 발생한다[86]. 아직 국내 의학사전에는 등록되어 있지 않은 감염증이다.
4.2.6. Blastocladiomyceta주로 수생 및 토양 환경에 서식하며, 대부분 종은 부생균 또는 절지동물 기생균으로 알려져 있다[87]. 형태학적 및 분자계통학적 연구에 따라, 가장 초기 분기한 균류 계통 중 하나로 Chytridiomycota에 속했지만, 독립된 문으로 인정되었다[88,89].
4.2.7. Chytridiomyceta
Chytridiomycota는 수생 및 토양환경에서 모두 분포한다. 대부분 부생균이지만 많은 경우 조류 기생체로도 존재한다[90]. 또한 일부 종은 양서류 피부를 감염시켜 치명적인 병인 chytridiomycosis를 유발한다. 전 세계적으로 양서류 개체군 감소와 멸종의 주요 원인이다[91–93]. 생활사 상으로 영양체 전체가 포자낭으로 전환하는 전실성(holocarpic) 형태와 영양체와 생식 구조가 분리되어 발달하는 분식성(eucarpic) 형태가 모두 보고되었다[94].
Neocallimastigomycota는 대형 초식동물의 소화관 내에 서식하는 혐기성 장내 균류이다[95]. 혐기성 환경에서 생존하며 에너지를 대사하기 때문에 미토콘드리아와 유사한 hydrogenosome을 가지고 있다[96]. Hydrogenosome은 포도당 같은 탄수화물을 분해하여 에너지를 생성하는 과정에서 수소를 생성한다. 또한 초식동물의 소화 과정에서 셀룰로오스와 같은 복잡한 식물성 물질을 분해하는 역할을 한다[97,98].
Monoblepharomycota는 전통적으로 Chytridiomycota에 포함되었으나, 분자계통학적 분석과 형태학적 특징에 근거하여 독립된 단일계통군으로 인정하였다[99]. 주로 담수 환경에서 발견되며, 육상 환경에서도 부생균으로 보고되었다[17,100]
4.2.8. Aphelidiomyceta (Aphelidiomycota)
Aphelidiomycota는 조류와 규조류에 기생한다[101,102]. 초기에는 Cryptomycota와 Microsporidia를 포함하는 Opisthosporidia의 일부로 분류되었으나, 후속 연구에서 독립된 문으로 인정하였다[14].
4.2.9. Cryptomycota (syn. Rozellomycota)
Cryptomycota는 세포벽이 없는 전실성 내생 기생균이다. 숙주는 Oomycota, Chytridiomycota, Blastocladiomycota, Basidiomycota, 녹조류 등 다양하며, 숙주 특이성을 보인다[103]. Cryptomycota와 Microsporidia의 위치는 균류 내 계통학에서 논쟁중이다. 여러 연구는 이 그룹이 균류 중 가장 먼저 초기 분지군으로 인식하였다[8,12,104]. 가장 먼저 분지된 계통 때문에 Cryptomycota는 균류의 기원과 초기 진화를 이해하는 핵심그룹으로 간주된다[103,105]. 일부 연구는 Cryptomycota와 Aphelidiomycota를 Opisthosporidia로 묶기도 했으나, 현재는 Cryptomycota를 균류 내 독립된 문으로 인정하였다[14].
4.2.10. Sanchytriomycota
Sanchytriomycota는 조류에 기생하는 단세포 균류로, 형태적으로 Chytridiomycota와 유사하나 분자계통학적으로 독립적인 계통이다[16]. Voigt et al. (2021)은 이를 단일 강, 목, 과, 2속을 포함하는 독립된 문으로 인정하였다[106]. 계통발생학적으로는 Blastocladiomycota의 자매군으로 위치하며, 편모의 보존, 퇴화 과정을 이해하는 데 중요한 위치를 차지한다. 상당수의 편모 관련 단백질(ciliome)을 상실했으나, 특정 tubulin polymerization promoting protein(TPPP)-유전자를 보유하여 편모 기원의 진화 연구에 중요한 단서를 제공한다[107].
최근의 계통유전체학 기반 분석 결과를 반영하여, 세계 주요 균류 데이터베이스인 MycoBank 및 Index Fungorum은 기존의 분류 체계를 넘어 Tedersoo et al. (2018)[14] 및 James et al. (2020)[15]의 고차 분류 체계를 적극 반영하고 있다. 특히 MycoBank는 각 문과 아계의 구분을 명확히 표시하였다. 예를 들면, Zygomycota의 해체 이후 신설된 Mucoromycota와 Zoopagomycota는 기존 문 수준에서 아계 수준으로 승격되어, MycoBank 상에서 독립된 상위 분류군으로 등재되었다. 국제 균류학 학술지들(Fungal Diversity, Studies in Mycology, Mycologia 등)은 2010년대 후반부터 계통유전체 기반 고등 분류 체계를 채택하고 있으며, 신종 보고 시 해당 체계에 따른 계통적 위치를 명시하는 것이 표준으로 자리 잡고 있다. 이는 향후 분류 체계의 혼란을 방지하고, 다양한 종의 비교·분석 및 생태학적 연구에 있어 일관된 기준을 제공하는 것을 목적으로 한다.
국내 전공 서적에서 제시하는 균류 분류 체계는 여전히 큰 불일치를 보인다. 일부 교재는 전통적인 4–5균문 체계(Ascomycota, Basidiomycota, Zygomycota, Chytridiomycota 등)를 유지하는 반면, 다른 교재는 6–7균문 체계로 확대하여 Glomeromycota, Neocallimastigomycota, Cryptomycota 등을 반영하고 있다. 최근 출판된 교재에서는 Mucoromycota와 Zoopagomycota를 독립된 문으로 구분하거나, Microsporidia의 계통학적 위치 논쟁을 언급하는 등 부분적으로 근래의 분류 체계를 수용하고 있으나, 여전히 문제점이 존재한다. 이러한 현황은 국내 교재들이 최신 계통유전체학 기반 분류를 충분히 반영하지 못하고 있음을 보여주며, 이를 통합·정리하는 작업이 필요하다. 국내에 출판된 전공 서적의 분류 체계 현황을 정리하여 Table 2에 제시하였다. 다계통성(polyphyly)이 입증되어 국제적으로 해체된 집단임에도, 여전히 다수의 국내 교재에서 Zygomycota가 하나의 독립 문으로 제시되었다. Zygomycosis 는 폐기된 용어로 간주하지만, 의학과 보건학 분야 임상 교재 일부에서 여전히 접합균증으로 사용되고 있다. 국제적으로는 Zygomycosis는 더 이상 사용되지 않으며, 이미 Mucormycosis와 Entomophthoromycosis로 구분하여 사용하는 것이 표준이다[118,119]. Microsporidia의 위치는 논쟁 중이다. 국제적으로는 Rozellomycota 내 자매군으로 보는 시각이 우세하지만, 아직 세부 계통을 안정적으로 나눌 근거가 부족하다[13]. 특히 최근 미국에서 2023년도에 간행된 Agrios’ Plant Pathology 6판의 경우도 기존 5판에 비해 식물균류병학 분야를 다루는 Chapter 7에서 새로운 분류 체계가 일부 반영되어 병원균 명이 기술되었다[43,109]. 그러나 아직 국명이 확립되지 않아 교육 현장에서 활용하는 데 어려움을 겪고 있다.
Table 2. The list of fungal phyla covered in university textbooks related to microbiology, plant pathology, and mycology written in Korean currently used in Korea
테이블
최근 계통유전체학의 발전은 진균계(Fungi)의 분류 체계를 획기적으로 재편하였다. 19문, 9아계 체계는 진균계 내 계통관계의 재정립 뿐 아니라, 새로운 문(phylum)의 독립성과 고등 균류(Dikarya)의 다양성을 보다 명확하게 설명할 수 있는 근거를 제공하였다. 이러한 진보는 진화적 관점 뿐만아니라 생태학, 병리학, 생물자원학 분야에도 실질적인 파급력을 가지며, 환경 시료 기반의 대사량 데이터 해석과 병원성 예측, 균류 생물다양성 평가의 정확도 향상으로 이어지고 있다.
그러나 한국은 여전히 4–7문 중심의 이전 분류 체계를 교육 및 연구에서 광범위하게 사용하고 있다. 국립생물자원관을 비롯한 주요 국가기관과 대학은 신종 보고와 미기록종 탐색에 힘쓰고 있으나, 실제 학술 및 교육 현장에서는 현대 분류 체계가 제대로 반영되지 않고 있어 지식의 전달과 해석에 혼란을 야기하고 있다. 특히, 전공 교육 교재와 국가 생물종 데이터베이스에서 최신 분류 체계를 반영하지 못하고 있어 학계와 실무 간의 괴리가 발생하고 있다. 균류분류의 전문가가 가장 많이 활동하고 분류논문이 가장 많이 발표되는 저널을 간행하는 한국균학회를 선두로 속히 신분류 체계를 적용하여 기존 분류 체계를 재정립하고 유관학회와 교육계에서 활용될 수 있도록 협력이 요구된다. 주요 추진 방향은 다음과 같다.
교육 자료의 개편: 대학 및 고등학교 수준의 균류 교육 교재에 최신 분류 체계를 반영.
데이터베이스 갱신: 국립생물자원관, 한반도생물다양성시스템의 주요 데이터베이스의 표준화 및 갱신.
학술 공론화: 한국균학회 및 관련 학회 차원에서 분류 체계 개정과 국명 논의.
국제 표준과의 연계: MycoBank, Index Fungorum, UNITE 등과의 동기화 및 협력.
균류 분류 체계의 최신화는 단지 분류학적 정확성의 확보를 넘어, 국가적 생물자원 주권 확보와도 직결된다. 따라서 향후 국내 학계는 계통유전체학적 접근을 적극 수용하고, 교육 및 정책 시스템 전반에 걸친 구조적 개선을 통해 조속히 국제 표준에 부합하는 균류 분류 체계를 확립해야 할 것이다.
본 논문은 농촌진흥청 연구사업(RS-2025-05962968)의 지원에 의해 이루어진 것임.
The authors declare no competing interests.
1. Coleine C, Stajich JE, Selbmann L. Fungi are key players in extreme ecosystems. Trends Ecol Evol 2022;37:517-28. https://doi.org/10.1016/j.tree.2022.02.002
[DOI]
2. Lange L. The importance of fungi and mycology for addressing major global challenges. IMA Fungus 2014;5:463-71. https://doi.org/10.5598/imafungus.2014.05.02.10
[DOI]
3. Zhou LW, May TW. Fungal taxonomy: Current status and research agendas for the interdisciplinary and globalisation era. Mycology 2023;14:52-9. https://doi.org/10.1080/21501203.2022.2103194
[DOI]
4. Nilsson RH, Anslan S, Bahram M, Wurzbacher C, Baldrian P, Tedersoo L. Mycobiome diversity: High-throughput sequencing and identification of fungi. Nat Rev Microbiol 2019;17:95-109. https://doi.org/10.1038/s41579-018-0116-y
[DOI]
5. Lücking R, Aime MC, Robbertse B, Miller AN, Ariyawansa HA, Aoki T, Schoch CL, Cardinali G, Crous P, Druzhinina I, et al. Unambiguous identification of fungi: Where do we stand and how accurate and precise is fungal DNA barcoding? IMA Fungus 2020;11:14. https://doi.org/10.1186/s43008-020-00033-z
[DOI]
6. Cavalier-Smith T. The origin of fungi and pseudofungi. In: Rayner ADM, Brasier CM, Moore D, editors. Evolutionary biology of the fungi. Cambridge: Cambridge University Press; 1987. p. 339-53.
7. McLaughlin DJ, Hibbett DS, Lutzoni F, Spatafora JW, Vilgalys R. The search for the fungal tree of life. Trends Microbiol 2009;17:488-97. https://doi.org/10.1016/j.tim.2009.08.001
[DOI]
8. James TY, Kauff F, Schoch CL, Matheny PB, Hofstetter V, Cox CJ, Celio G, Gueidan C, Fraker E, Miadlikowska J, et al. Reconstructing the early evolution of Fungi using a six-gene phylogeny. Nature 2006;443:818-22. https://doi.org/10.1038/nature05110
[DOI]
9. Viswanath B, Rajesh B, Janardhan A, Kumar AP, Narasimha G. Fungal laccases and their applications in bioremediation. Enzyme Res 2014;2014:163242. https://doi.org/10.1155/2014/163242
[DOI]
10. Zhang N, Luo J, Bhattacharya D. Advances in fungal phylogenomics and their impact on fungal systematics. Adv Genet 2017;100:309-28. https://doi.org/10.1016/bs.adgen.2017.09.004
[DOI]
11. Pizarro D, Divakar PK, Grewe F, Leavitt SD, Huang JP, Dal Grande F, Schmitt I, Wedin M, Crespo A, Lumbsch T. Phylogenomic analysis of 2556 single-copy protein-coding genes resolves most evolutionary relationships for the major clades in the most diverse group of lichen-forming fungi. Fungal Divers 2018;92:31-41. https://doi.org/10.1007/s13225-018-0407-7
[DOI]
12. Hibbett DS, Binder M, Bischoff JF, Blackwell M, Cannon PF, Eriksson OE, Huhndorf S, James T, Kirk PM, Zhang N, et al. A higher-level phylogenetic classification of the Fungi. Mycol Res 2007;111:509-47. https://doi.org/10.1016/j.mycres.2007.03.004
[DOI]
13. Spatafora JW, Chang Y, Benny GL, Lazarus K, Smith ME, Berbee ML, Bonito G, Corradi N, Grigriev I, Stajich JE, et al. A phylum-level phylogenetic classification of zygomycete fungi based on genome-scale data. Mycologia 2016;108:1028-46. https://doi.org/10.3852/16-042
[DOI]
14. Tedersoo L, Sánchez-Ramírez S, Koljalg U, Bahram M, Döring M, Schigel D, May T, Ryberg M, Abarenkov K. High-level classification of the Fungi and a tool for evolutionary ecological analyses. Fungal Divers 2018;90:135-59. https://doi.org/10.1007/s13225-018-0401-0
[DOI]
15. James TY, Stajich JE, Hittinger CT, Rokas A. Toward a fully resolved fungal tree of life. Annu Rev Microbiol 2020;74:291-313. https://doi.org/10.1146/annurev-micro-022020-051835
[DOI]
16. Galindo LJ, López-García P, Torruella G, Karpov S, Moreira D. Phylogenomics of a new fungal phylum reveals multiple waves of reductive evolution across Holomycota. Nat Commun 2021;12:4973. https://doi.org/10.1038/s41467-021-25308-w
[DOI]
17. Wijayawardene N, Hyde KD, Mikhailov KV, Péter G, Aptroot A, Pires-Zottarelli CL, Goto BT, Tokarev Y, Haelewaters D, Karpov SA. Classes and phyla of the kingdom Fungi. Fungal Divers 2024;128:1-165. https://doi.org/10.1007/s13225-024-00540-z
[DOI]
18. Hawksworth DL, Lücking R. Fungal diversity revisited: 2.2 to 3.8 million species. Microbiol Spectr 2017;5. https://doi.org/10.1128/microbiolspec.FUNK-0052-2016
[DOI]
19. Yahr R, Schoch CL, Dentinger BT. Scaling up discovery of hidden diversity in fungi. Philos Trans R Soc Lond B Biol Sci 2016;371:20150336. https://doi.org/10.1098/rstb.2015.0336
[DOI]
20. Linnaeus C. Species plantarum. Berlin: Impensis GC Nauk; 1799.
21. Naranjo-Ortiz MA, Gabaldón T. Fungal evolution: Major ecological adaptations and evolutionary transitions. Biol Rev 2019;94:1443-76. https://doi.org/10.1111/brv.12510
[DOI]
22. Ronald AR, Alfa MJ. Microbiology of the genitourinary system. In: Baron S, editor. Medical microbiology. 4th ed. Galveston (TX): University of Texas Medical Branch at Galveston; 1996.
23. Guarro J, Gene J, Stchigel AM. Developments in fungal taxonomy. Clin Microbiol Rev 1999;12:454-500. https://doi.org/10.1128/CMR.12.3.454
[DOI]
24. Schüßler A, Schwarzott D, Walker C. A new fungal phylum, the Glomeromycota: Phylogeny and evolution. Mycol Res 2001;105:1413-21. https://doi.org/10.1017/S0953756201005196
[DOI]
25. Muszewska A, Pawłowska J, Krzyściak P. Biology, systematics, and clinical manifestations of Zygomycota infections. Eur J Clin Microbiol Infect Dis 2014;33:1273-87. https://doi.org/10.1007/s10096-014-2076-0
[DOI]
26. Kwon-Chung KJ. Taxonomy of fungi causing mucormycosis and entomophthoramycosis. Clin Infect Dis 2012;54:S8-S15. https://doi.org/10.1093/cid/cir864
[DOI]
27. Hane JK, Rouxel T, Howlett BJ, Kema GH, Goodwin SB, Oliver RP. A novel mode of chromosomal evolution peculiar to filamentous Ascomycete fungi. Genome Biol 2011;12:R45. https://doi.org/10.1186/gb-2011-12-5-r45
[DOI]
28. Keeling PJ. Congruent evidence from α-tubulin and β-tubulin gene phylogenies for a zygomycete origin of microsporidia. Fungal Genet Biol 2003;38:298-309. https://doi.org/10.1016/S1087-1845(02)00537-6
[DOI]
29. Salgado JFM, Quandt CA, Stajich JE. Phylogenetics and phylogenomics to understand fungal diversity. Authorea 2023. https://doi.org/10.22541/au.167845826.61933731/v1
[DOI]
30. Wang Y, Chang Y, Ortañez J, Peña JF, Carter-House D, Reynolds NK, Smith ME, Benny G, Mondo SJ, Stajich JE, et al. Divergent evolution of early terrestrial fungi reveals the evolution of mucormycosis pathogenicity factors. Genome Biol Evol 2023;15:evad046. https://doi.org/10.1093/gbe/evad046
[DOI]
31. Tahiri G, Lax C, Canovas-Marquez JT, Carrillo-Marin P, Sanchis M, Navarro E, Garre V, Nicolas FE. Mucorales and mucormycosis: Recent insights and future prospects. J Fungi 2023;9:335. https://doi.org/10.3390/jof9030335
[DOI]
32. Liu M, Lin L, Gebremariam T, Luo G, Skory CD, French SW, Chou TF, Edwards JE, Ibrahim AS. Fob1 and Fob2 proteins are virulence determinants of Rhizopus oryzae. PLoS Pathog 2015;11:e1004842. https://doi.org/10.1371/journal.ppat.1004842
[DOI]
33. Pérez-Arques C, Navarro-Mendoza MI, Murcia L, Navarro E, Garre V, Nicolás FE. A noncanonical RNAi pathway controls virulence and genome stability in Mucorales. PLoS Genet 2020;16:e1008611. https://doi.org/10.1371/journal.pgen.1008611
[DOI]
34. Szebenyi C, Gu Y, Gebremariam T, Kocsubé S, Kiss-Vetráb S, Jáger O, Patai R, Spisák K, Rita S, Papp T. CotH genes are necessary for virulence in Mucor lusitanicus. mBio 2023;14:e03386-22. https://doi.org/10.1128/mbio.03386-22
[DOI]
35. Wang H, Luo G, Hu X, Xu G, Wang T, Liu M, Qiu X, Fu J, Feng B, Li J. Targeting C/EBPα improves efficacy of FLT3 inhibitors in leukemia. Nat Commun 2023;14:1882. https://doi.org/10.1038/s41467-023-37381-4
[DOI]
36. Bauer R, Garnica S, Oberwinkler F, Riess K, Weiß M, Begerow D. Entorrhizomycota: A new fungal phylum. PLoS One 2015;10:e0128183. https://doi.org/10.1371/journal.pone.0128183
[DOI]
37. Karpov SA, Mamkaeva MA, Benzerara K, Moreira D, López-García P. Molecular phylogeny of Aphelidium aff. melosirae. Protist 2014;165:512-26. https://doi.org/10.1016/j.protis.2014.05.003
[DOI]
38. Jones MD, Richards TA, Hawksworth DL, Bass D. Validation of the phylum Cryptomycota. IMA Fungus 2011;2:173-5. https://doi.org/10.5598/imafungus.2011.02.02.08
[DOI]
39. James TY, Berbee ML. Newly described zoosporic fungi lacking a cell wall during trophic phase. Bioessays 2012;34:94-102. https://doi.org/10.1002/bies.201100110
[DOI]
40. Tindall BJ. Validly published vs legitimate names in prokaryote nomenclature. Int J Syst Evol Microbiol 2016;66:4905-6. https://doi.org/10.1099/ijsem.0.001420
[DOI]
41. Voglmayr H, Fournier J, Jaklitsch WM. Two new classes of Ascomycota. Persoonia 2019;42:36-49. https://doi.org/10.3767/persoonia.2019.42.02
[DOI]
42. Wang QM, Yurkov AM, Göker M, Lumbsch HT, Leavitt SD, Groenewald M, Theelen B, Liu XZ, Boekhout T, Bai FY. Phylogenetic classification of yeasts. Stud Mycol 2015;81:149-89. https://doi.org/10.1016/j.simyco.2015.12.002
[DOI]
43. Agrios GN. Agrios’ plant pathology (Korean edition). 5th ed. Seoul: World Science Co.; 2006.
44. Díaz-Escandón D, Tagirdzhanova G, Vanderpool D, Allen CC, Aptroot A, Češka O, Hawksworth DL, Huereca A, Knudsen K, Spribille T. Genome-level analyses resolve an ancient lineage of symbiotic ascomycetes. Curr Biol 2022;32:5209-18. https://doi.org/10.1016/j.cub.2022.11.014
[DOI]
45. Mishra B, Choi YJ, Thines M. Phylogenomics of Bartheletia paradoxa reveals basal position in Agaricomycotina. Mycol Prog 2018;17:333-41. https://doi.org/10.1007/s11557-017-1349-2
[DOI]
46. Čadež N, Dlauchy D, Tome M, Péter G. Novakomyces olei sp. nov. Microorganisms 2021;9:301. https://doi.org/10.3390/microorganisms9020301
[DOI]
47. Groenewald M, Hittinger CT, Bensch K, Opulente DA, Shen XX, Li Y, Liu C, Labella AL, Zhou X, Rokas A. Genome-informed classification of Saccharomycotina. Stud Mycol 2023;105:1-22. https://doi.org/10.3114/sim.2023.105.01
[DOI]
48. Branco S. Fungal diversity-an overview. In: Grillo O, Venora G, editors. Biodiversity. Rijeka: InTech; 2011. https://doi.org/10.5772/23975
[DOI]
49. Cavalier-Smith T. A revised six-kingdom system of life. Biol Rev 1998;73:203-66. https://doi.org/10.1017/S0006323198005167
[DOI]
50. Neiman AM. Ascospore formation in Saccharomyces cerevisiae. Microbiol Mol Biol Rev 2005;69:565-84. https://doi.org/10.1128/MMBR.69.4.565-584.2005
[DOI]
51. Levin SA. Encyclopedia of biodiversity. Waltham: Academic Press; 2013.
52. Bennett RJ, Turgeon BG. Fungal sex: The Ascomycota. Microbiol Spectr 2016. https://doi.org/10.1128/microbiolspec.FUNK-0005-2016
[DOI]
53. Bhunia AK. Foodborne microbial pathogens. New York: Springer; 2018. https://doi.org/10.1007/978-1-4939-7349-1_8
[DOI]
54. Keller NP. Fungal secondary metabolism. Nat Rev Microbiol 2019;17:167-80. https://doi.org/10.1038/s41579-018-0121-1
[DOI]
55. Berbee ML. Phylogeny of plant and animal pathogens in Ascomycota. Physiol Mol Plant Pathol 2001;59:165-87. https://doi.org/10.1006/pmpp.2001.0355
[DOI]
56. Taylor TN, Krings M, Taylor EL. Fossil fungi. London: Academic Press; 2014. https://doi.org/10.1016/B978-0-12-387731-4.00009-8
[DOI]
57. Duplessis S, Cuomo CA, Lin YC, Aerts A, Tisserant E, Veneault-Fourrey C, David LJ, Hacquard S, Amselem J, Martin F. Genomic analysis of rust fungi. Proc Natl Acad Sci USA 2011;108:9166-71. https://doi.org/10.1073/pnas.1019315108
[DOI]
58. Floudas D, Binder M, Riley R, Barry K, Blanchette RA, Henrissat B, Martínez AT, Otillar R, Spatafora JW, Hibbett DS. Paleozoic origin of lignin decomposition. Science 2012;336:1715-9. https://doi.org/10.1126/science.1221748
[DOI]
59. Riley R, Salamov A, Brown DW, Nagy LG, Floudas D, Held BW, Levasseur A, Lombard V, Morin E, Grigoriev IV. Basidiomycete genome sampling and wood decay evolution. Proc Natl Acad Sci USA 2014;111:9923-8. https://doi.org/10.1073/pnas.1400592111
[DOI]
60. Cairney JW. Basidiomycete mycelia in forest soils. Mycol Res 2005;109:7-20. https://doi.org/10.1017/S0953756204001753
[DOI]
61. Ghobad-Nejhad M, Dima B, Cui BK, Si J. Basidiomycete fungi: From biosystematics and biodiversity to biotechnology. Front Microbiol 2023;14:1128319. https://doi.org/10.3389/fmicb.2023.1128319
[DOI]
62. Lacaz CDS, Heins-Vaccari EM, Melo NTD, Hernandez-Arriagada GL. Basidiomycosis: A review of the literature. Rev Inst Med Trop Sao Paulo 1996;38:379-90. https://doi.org/10.1590/S0036-46651996000500011
[DOI]
63. Tam SY, Uchida K, Enomoto H, Takahashi S, Makimura K, Sakuda S. A new metabolite produced by Schizophyllum commune. J Antibiot 2022;75:243-6. https://doi.org/10.1038/s41429-022-00511-z
[DOI]
64. Wargo PM, Shaw CI. Armillaria root rot: The puzzle is being solved. Plant Dis 1985;69:826-32. https://doi.org/10.1094/PD-69-826
[DOI]
65. Deacon J. Fungal biology (Korean edition). 4th ed. Seoul: World Science Co.; 2006.
66. Jennessen J, Schnürer J, Olsson J, Samson RA, Dijksterhuis J. Morphological characteristics of sporangiospores of Rhizopus oligosporus. Mycol Res 2008;112:547-63. https://doi.org/10.1016/j.mycres.2007.11.006
[DOI]
67. Ribes JA, Vanover-Sams CL, Baker DJ. Zygomycetes in human disease. Clin Microbiol Rev 2000;13:236-301. https://doi.org/10.1128/CMR.13.2.236
[DOI]
68. Gomes MZR, Lewis RE, Kontoyiannis DP. Mucormycosis caused by unusual mucormycetes. Clin Microbiol Rev 2011;24:411-45. https://doi.org/10.1128/CMR.00056-10
[DOI]
69. Summerbell RC. Root endophyte and mycorrhizosphere fungi of black spruce. Stud Mycol 2005;53:121-45. https://doi.org/10.3114/sim.53.1.121
[DOI]
70. Hirose D, Degawa Y, Inaba S, Tokumasu S. The anamorphic genus Calcarisporiella. Mycoscience 2012;53:256-60. https://doi.org/10.47371/S10267-011-0160-1
[DOI]
71. Voigt K, Kirk PM. Classification of Zygomycetes. In: Encyclopedia of food microbiology. London: Academic Press; 2014. https://doi.org/10.1016/B978-0-12-384730-0.00136-1
[DOI]
72. Sherchan R, Zahra F. Entomophthoromycosis. StatPearls; 2025.
73. Moss ST, Lichtwardt RW. Development of trichospores in Genistellospora homothallica. Can J Bot 1976;54:2346-64. https://doi.org/10.1139/b76-251
[DOI]
74. Liimatainen K. Nomenclatural novelties 185. Index Fungorum 2014;185.
75. Barr DJ. Reclassification of the Chytridiales. Can J Bot 1980;58:2380-94. https://doi.org/10.1139/b80-276
[DOI]
76. Kirk PM, Cannon PF, Minter DW, Stalpers JA. Dictionary of the fungi. 10th ed. Wallingford: CABI; 2008. https://doi.org/10.1079/9780851998268.0000
[DOI]
77. Powell MJ, Letcher PM. Chytridiomycota and related groups. In: Systematics and evolution of fungi. Berlin: Springer; 2014. https://doi.org/10.1007/978-3-642-55318-9_6
[DOI]
78. Taylor SK, Williams ES, Mills KW. Mortality of captive Canadian toads from Basidiobolus ranarum. J Wildl Dis 1999;35:64-9. https://doi.org/10.7589/0090-3558-35.1.64
[DOI]
79. Marclay M, Langohr IM, Gaschen FP, Rodrigues-Hoffmann A, Carossino M, Stewart MA, Myers AN, Grooters AM. Colorectal basidiobolomycosis in a dog. J Vet Intern Med 2020;34:2091-5. https://doi.org/10.1111/jvim.15859
[DOI]
80. Porto E, Milanez AI. Basidiobolus isolated from reptiles and amphibians in Brazil. Rev Inst Med Trop Sao Paulo 1979;21:237-45.
81. Seyedmousavi S, Guillot J, Tolooe A, Verweij PE, De Hoog GS. Neglected fungal zoonoses. Clin Microbiol Infect 2015;21:416-25. https://doi.org/10.1016/j.cmi.2015.02.031
[DOI]
82. Zavasky DM, Samowitz W, Loftus T, Segal H, Carroll K. Gastrointestinal zygomycotic infection caused by Basidiobolus ranarum. Clin Infect Dis 1999;28:1244-8. https://doi.org/10.1086/514781
[DOI]
83. Sethy M, Sahu S, Sachan S. Basidiobolomycosis case report. Indian Dermatol Online J 2021;12:307-11. https://doi.org/10.4103/idoj.IDOJ_456_20
[DOI]
84. Gugnani HC. Zygomycosis due to Basidiobolus ranarum. Eur J Epidemiol 1999;15:923-9. https://doi.org/10.1023/A:1007656818038
[DOI]
85. Zekavat OR, Abdolkarimi B, Pouladfar G, Fathpour G, Mokhtari M, Shakibazad N. Colonic basidiobolomycosis case report. Rev Soc Bras Med Trop 2017;50:712-4. https://doi.org/10.1590/0037-8682-0057-2017
[DOI]
86. Al Yazidi L, Al Sinani S, Al Adawi B, Al Riyami M, Wali Y, Al Rawas A, Al Musalhi B, Meis JF, Housni SA, Al Hatmi AMS. Disseminated basidiobolomycosis case report. Mycopathologia 2024;189:12. https://doi.org/10.1007/s11046-023-00820-3
[DOI]
87. Money NP. Fungal diversity. In: The fungi. London: Academic Press; 2015. https://doi.org/10.1016/B978-0-12-382034-1.00001-3
[DOI]
88. James TY, Letcher PM, Longcore JE, Mozley-Standridge SE, Porter D, Powell MJ, Griffith GW, Vilgalys R. Molecular phylogeny of the flagellated fungi. Mycologia 2006;98:860-71. https://doi.org/10.1080/15572536.2006.11832616
[DOI]
89. Porter TM, Martin W, James TY, Longcore JE, Gleason FH, Adler PH, Vilgalys R. Molecular phylogeny of Blastocladiomycota. Fungal Biol 2011;115:381-92. https://doi.org/10.1016/j.funbio.2011.02.004
[DOI]
90. Seto K, Degawa Y. Pendulichytrium sphaericum gen. et sp. nov. Mycoscience 2018;59:59-66. https://doi.org/10.1016/j.myc.2017.08.004
[DOI]
91. Kilpatrick AM, Briggs CJ, Daszak P. Ecology of chytridiomycosis. Trends Ecol Evol 2010;25:109-18. https://doi.org/10.1016/j.tree.2009.07.011
[DOI]
92. Grogan LF, Robert J, Berger L, Skerratt LF, Scheele BC, Castley JG, Newell DA, McCallum HI. Amphibian immune response to chytridiomycosis. Front Immunol 2018;9:2536. https://doi.org/10.3389/fimmu.2018.02536
[DOI]
93. Van Rooij P, Martel A, Haesebrouck F, Pasmans F. Amphibian chytridiomycosis review. Vet Res 2015;46:137. https://doi.org/10.1186/s13567-015-0266-0
[DOI]
94. Krings M, Dotzler N, Galtier J, Taylor TN. Microfungi from the Mississippian of France. Rev Palaeobot Palynol 2009;156:319-28. https://doi.org/10.1016/j.revpalbo.2009.03.011
[DOI]
95. Murphy CL, Youssef NH, Hanafy RA, Couger MB, Stajich JE, Wang Y, Baker K, Dagar SS, Griffith GW, Elshahed MS. Horizontal gene transfer in Neocallimastigomycota. Appl Environ Microbiol 2019;85:e00988-19. https://doi.org/10.1128/AEM.00988-19
[DOI]
96. Hackstein JH, Baker SE, van Hellemond JJ, Tielens AG. Hydrogenosomes of anaerobic fungi. Springer; 2020. https://doi.org/10.1007/978-3-030-17941-0_7
[DOI]
97. Kameshwar AKS, Qin W. Genome-wide analysis of Neocallimastigomycota fungi. J Genomics 2018;6:74. https://doi.org/10.7150/jgen.25648
[DOI]
98. Wilken SE, Monk JM, Leggieri PA, Lawson CE, Lankiewicz TS, Seppälä S, Daum CG, Jenkins J, Lipzen AM, O’Malley MA. Genome-scale metabolic model of anaerobic fungi. mSystems 2021;6:e00002-21. https://doi.org/10.1128/mSystems.00002-21
[DOI]
99. Dee JM, Mollicone M, Longcore JE, Roberson RW, Berbee ML. Cytology of Monoblepharidomycetes. Mycologia 2025;107:710-28. https://doi.org/10.3852/14-275
[DOI]
100. Karpov SA, Mamanazarova KS, Popova OV, Aleoshin VV, James TY, Mamkaeva MA, Tcvetkova VS, Vishnyakov AE, Longcore JE. Monoblepharidomycetes diversity. Fungal Biol 2017;121:729-41. https://doi.org/10.1016/j.funbio.2017.05.002
[DOI]
101. Gromov BV. Aphelidium tribonemae parasitizing yellow-green algae. Mikol Fitopatol 1972;6:443-5.
102. Karpov SA, Tcvetkova VS, Mamkaeva MA, Torruella G, Timpano H, Moreira D, López-García P. Morphological diversity of Opisthosporidia. J Eukaryot Microbiol 2017;64:204-12. https://doi.org/10.1111/jeu.12352
[DOI]
103. Letcher PM, Longcore JE, James TY, Leite DS, Simmons DR, Powell MJ. Rozella multimorpha. J Eukaryot Microbiol 2018;65:180-90. https://doi.org/10.1111/jeu.12452
[DOI]
104. Corsaro D, Walochnik J, Venditti D, Steinmann J, Müller KD, Michel R. Microsporidia-like parasites of amoebae. Parasitol Res 2014;113:1909-18. https://doi.org/10.1007/s00436-014-3838-4
[DOI]
105. Letcher PM, Powell MJ. Taxonomic revision of Rozella. IMA Fungus 2018;9:383-99. https://doi.org/10.5598/imafungus.2018.09.02.09
[DOI]
106. Voigt K, James TY, Kirk PM, Santiago ALDA, Waldman B, Griffith GW, Fu M, Radek R, Strassert JFH, Lee HB, et al. Early-diverging fungal phyla. Fungal Divers 2021;109:59-98. https://doi.org/10.1007/s13225-021-00480-y
[DOI]
107. Orosz F. Sanchytriomycota parasitic fungi. Microorganisms 2023;11:2029. https://doi.org/10.3390/microorganisms11082029
[DOI]
108. Watkinson SC, Boddy L, Money NP. The fungi (Korean edition). 3rd ed. Seoul: World Science; 2017.
109. Agrios GN. Agrios’ plant pathology. 6th ed. Academic Press; 2024.
110. Madigan MT, Bender KS, Buckley DH. Brock biology of microorganisms (Korean edition). 15th ed. Seoul: Bioscience; 2020.
111. Nester EW, Anderson DG, Roberts CE. Nester’s microbiology (Korean edition). 8th ed. Paju: Donghwa Technology Publishing; 2015.
112. The Korean Society for Microbiology. Microbiology concepts and connections. Seoul: Bummun Education; 2020.
113. Chess B. Foundations in microbiology (Korean edition). 11th ed. Seoul: LifeScience; 2021.
114. Willey JM, Sandman K, Wood D. Prescott’s microbiology (Korean edition). 12th ed. Paju: Gyomun; 2023.
115. Chess B. Talaro foundations in microbiology (Korean edition). 12th ed. Paju: Gyomun; 2025.
116. Bauman RW. Bauman hospital microbiology (Korean edition). 12th ed. Seoul: Bioscience; 2015.
117. Kim YG, Kwon PS, Kim SH, Kim SH, Kim JH, Ryu JG, Park M, Park SM, Park ES, Park HH. Clinical mycology. 5th ed. Seoul: Korea Med Books; 2021.
118. Acosta-España JD, Voigt K. Entomophthoromycosis versus mucormycosis. Front Microbiol 2022;13:1035100. https://doi.org/10.3389/fmicb.2022.1035100
[DOI]
119. Shaikh N, Hussain KA, Petraitiene R, Schuetz AN, Walsh TJ. Entomophthoramycosis: A neglected tropical mycosis. Clin Microbiol Infect 2016;22:688-94. https://doi.org/10.1016/j.cmi.2016.04.005
[DOI]