Seong-Hwan Kim1,2,3, Jun-Woo Choi1, Seong-Keun Lim1, Chang-Gi Back4, Seung-Yeol Lee1,2,5,*, and Hee-Young Jung1,2,5
1Department of Plant Medicine, Kyungpook National University, Daegu 41566, Korea
2Department of Plant Protection and Quarantine, Graduate School of Plant Protection and Quarantine, Kyungpook National University, Daegu 41566, Korea
3Cheongsol Tree Hospital Co., Ltd., Daegu 42795, Korea
4Department of Environmental Horticulture and Landscape Architecture, Dankook University, Cheonan 31116, Korea
5Institute of Plant Medicine, Kyungpook National University, Daegu 41566, Korea
*Correspondence to leesy1123@knu.ac.kr
Korean Journal of Mycology (Kor J Mycol) 2026 March, Volume 54, Issue 1, pages 19-31.
https://doi.org/10.4489/kjm.2026.54.1.3
Received on January 13, 2026, Revised on March 13, 2026, Accepted on March 16, 2026, Published on March 31, 2026.
Copyright © The Korean Society of Mycology.
This is an Open Access article which is freely available under the Creative Commons Attribution-Non-Commercial 4.0 International License (CC BY-NC) (https://creativecommons.org/licenses/by-nc/4.0/).
Roses (Rosa spp.) are widely cultivated as ornamental plants in both Korea and worldwide. However, black spot disease caused by Diplocarpon rosae (= Marssonina rosae) continues to result in considerable damage in commercial production. While investigating black spot disease of roses collected from 27 regions across Korea, fungal strains were isolated from abnormal leaves exhibiting black spot symptoms to examine their distribution and characteristics. Regardless of region or cultivar, all isolates exhibited similar morphology, characterized by dark brown to black acervuli on symptomatic rose leaves and hyaline, two-celled conidia. The morphological characteristics of the representative strain KNUF-24-DG, including conidial size (16.5–25.8 × 4.7–6.5 µm) and cultural characteristics on potato dextrose agar, were similar to those previously described for D. rosae. For phylogenetic analyses of the 27 fungal strains, the internal transcribed spacer (ITS) regions and large subunit (LSU) rRNA gene were amplified. The ITS region showed 97.7–100% similarity to D. rosae strains CBS 163.31, CFCC 6814, KACC 42437, and DKU017, and the LSU gene sequences exhibited 99.6% and 100% similarities with D. rosae CBS 163.31 and CBS 829.72, respectively, indicating high sequence similarity to D. rosae strains in both molecular markers. Based on cultural, morphological, and phylogenetic analyses, 27 fungal strains were identified as D. rosae.
Diplocarpon rosae, Korea, Rosa spp., Rose black spot disease
장미(Rosa spp.)는 전 세계적으로 널리 재배되는 대표적인 관상식물로, 절화류로 유통되거나 공공시설 및 조경 공간에 식재되어 미관을 향상시키는 데 활용된다[1]. 국내에서는 핑크피스, 아이스버그, 심파시, 퀸 엘리자베스, 루주메이양 등 다양한 장미 품종이 재배되고 있으며, 2022년 기준 식재 면적은 약 226 ha, 판매량은 1억 1,100만 본, 연간 매출액은 약 617억 원에 달해 절화류 중 가장 높은 시장 점유율을 기록하고 있다[2]. 또한 장미는 국민적 선호도가 높은 화종으로서 지자체 주도의 공원 조성 및 장미 축제 개최 등을 통해 지역 홍보와 경제 활성화에 활용되고 있다. 그러나 장미는 다양한 병원균에 의해 생육 전반에 걸쳐 병해에 노출되기 쉬운 관상식물로 현재까지 국내에서는 곰팡이와 세균에 의해 총 11종의 병이 보고되어 있으며, 이 중 주요한 진균병으로는 Podosphaera pannosa에 의한 흰가루병, Botrytis cinerea에 의한 잿빛곰팡이병, Colletotrichum gloeosporioides에 의한 탄저병, Peronospora sparsa에 의한 노균병, 그리고 Diplocarpon rosae (= Marssonina rosae)에 의한 검은무늬병 등이 보고되어 있다[3]. 그 중 Diplocarpon rosae에 의한 장미 검은무늬병은 1815년 스웨덴에서 처음으로 발생이 보고된 이래, 1827년 벨기에를 비롯해 유럽 전역으로 확산되었으며, 북미에서는 1831년, 남미에서는 1880년, 호주에서는 1892년, 아프리카 및 중국에서는 1920년에 발생이 보고되는 등 다양한 기후와 지역에서 장미 검은무늬병의 발생이 지속적으로 보고되었다[4]. 장미 검은무늬병의 주요 증상은 잎과 잎자루에 검은 병반을 형성하여 조기 낙엽 및 낙화 피해를 유발하며, 장미의 전 생육기에 걸쳐 발생하고 묘목과 성목에서도 피해를 준다[5]. 특히 강우나 바람과 같은 환경적 요인에 의해 빠르게 확산되며, 피해가 장기간 지속되는 것이 특징으로 장미 검은무늬병 피해 발생 시 장미의 관상적 가치가 크게 저하되며 농가 및 시설 운영에 경제적 손실을 초래할 수 있다[5,6]. 국내 장미 검은무늬병에 대해서는 원인균인 D. rosae의 형태적 특징을 중심으로 제한적인 연구만 이루어졌으며, 국내에 분포하는 장미 검은무늬병 균주의 배양학적 특징과 분자계통학적 유연관계에 대한 연구는 부족한 실정이다[7]. 이에 본 연구에서는 국내 27개 지역에서 채집한 장미 검은무늬병 이병 시료로부터 병원균을 분리하고, 확보한 균주의 형태학적 및 배양학적 특성을 관찰하였다. 아울러 계통학적 유연관계를 분석함으로써, 국내 장미검은무늬병균의 분포 및 특성을 규명하고자 하였다.
2023년 9월부터 11월까지 국내 27개 지역에서 장미 검은무늬병 이병 시료를 채집하였다(Table 1 and Fig. 1). 채집 대상은 잎 전체에 짙은 갈색에서 검은색의 반점이 형성되고 낙엽 현상이 나타나는 등 일반적으로 알려진 장미 검은무늬병의 병징이 관찰되는 잎을 시료로 선정하였으며, 이병 조직은 정상적으로 생육한 잎과 명확하게 구분되었다[8]. 채집된 시료는 즉시 지퍼백에 밀봉한 후, 병원균 분리 배양 전까지 4°C에서 보관하였다. 병원균 분리는 기존에 보고된 사과갈색무늬병균(Marssonina coronaria = Diplocarpon coronariae)의 단포자 분리법을 참고하여 수행하였다[9]. 지역별로 확보된 단일 균총의 곰팡이 중에서 장미검은무늬병균과 배양학적 특징이 유사한 균주를 1개씩 선정하여 대표 균주로 지정하였으며, 실험을 위해 새로운 PDA (potato dextrose agar; Difco, Detroit, MI, USA) 배지에 계대 배양한 뒤 25°C에서 배양하였다.
Table 1. Strain name and sampling place with GPS information in South Korea
| Strain name | Region | Abbreviation | GPS information |
|---|---|---|---|
| KNUF-24-AD | Andong | AD | 36°35’20.4″N 128°37’11.9″E |
| KNUF-24-CA | Cheonan | CA | 36°50’14.7″N 127°10’21.0″E |
| KNUF-24-ChJ | Cheongju | ChJ | 36°37’07.7″N 127°30’39.2″E |
| KNUF-24-CJ | Chungju | CJ | 36°57’50.8″N 127°55’28.1″E |
| KNUF-24-CW | Changwon | CW | 35°12’24.9″N 128°41’28.2″E |
| KNUF-24-DG | Daegu | DG | 35°53’26.3″N 128°36’29.5″E |
| KNUF-24-DJ | Daejeon | DJ | 36°22’02.8″N 127°23’14.7″E |
| KNUF-24-DY | Danyang | DY | 36°58’34.7″N 128°21’28.4″E |
| KNUF-24-GC | Gochang | GC | 35°22’25.1″N 126°38’55.4″E |
| KNUF-24-GJ | Gwangju | GJ | 35°09’33.7″N 126°51’16.8″E |
| KNUF-24-GM | Gumi | GM | 36°05’57.8″N 128°24’07.5″E |
| KNUF-24-GN | Gangleung | GN | 37°45’42.1″N 128°54’21.7″E |
| KNUF-24-GoS | Gokseong | GoS | 35°16’53.2″N 127°18’09.3″E |
| KNUF-24-GS | Gunsan | GS | 35°57’38.3″N 126°42’57.0″E |
| KNUF-24-HC | Habcheon | HC | 35°33’35.7″N 128°09’19.1″E |
| KNUF-24-HD | Hadong | HD | 35°06’40.0″N 127°52’46.7″E |
| KNUF-24-JJ | Jeonju | JJ | 35°52’14.9″N 127°03’11.5″E |
| KNUF-24-NW | Namwon | NW | 35°24’41.7″N 127°22’18.5″E |
| KNUF-24-NYJ | Namyangju | NYJ | 37°39’18.4″N 127°10’38.1″E |
| KNUF-24-PC | Pocheon | PC | 37°55’25.7″N 127°14’25.0″E |
| KNUF-24-PH | Pohang | PH | 36°03’42.5″N 129°22’52.4″E |
| KNUF-24-SC | Samcheok | SC | 37°25’58.5″N 129°10’41.4″E |
| KNUF-24-SJ | Sangju | SJ | 36°34’37.9″N 128°09’39.1″E |
| KNUF-24-SoC | Sokcho | SoC | 38°12’54.6″N 128°34’54.2″E |
| KNUF-24-UJ | Uljin | UJ | 36°40’49.6″N 129°26’36.1″E |
| KNUF-24-US | Ulsan | US | 35°31’41.9″N 129°16’53.0″E |
| KNUF-24-YD | Yeongdong | YD | 36°12’43.0″N 127°59’43.5″E |
GPS: Global positioning system.
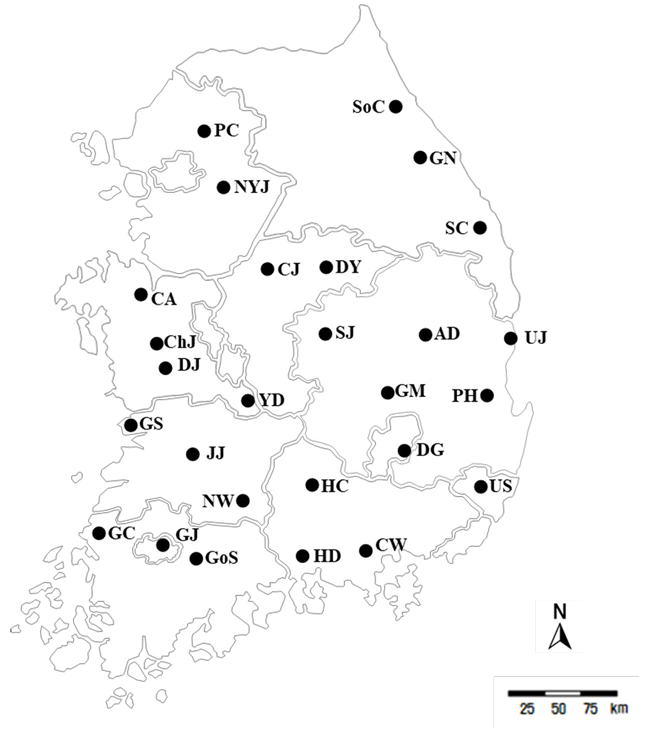
Fig. 1. Sampling locations of rose (Rosa spp.) leaf samples showing black spot symptoms in Korea. Abbreviations beside the circles correspond to those listed in Table 1.
이병 시료 표면에 형성된 병징 및 표징으로부터 실체현미경(DIMIS-M5; Olympus, Tokyo, Japan)과 광학현미경(BX-50; Olympus, Tokyo, Japan)을 이용하여 병원균의 형태학적 특징을 관찰하였다. 배양학적 특징의 경우, 지역별 대표 균주들을 이전 연구 방법을 따라 각각 25°C에서 28일 동안 PDA 배지에 배양하고 형성된 균체를 관찰하였다[10].
분자생물학적 동정을 위해 선발된 균주로부터는 HiGene™ Genomic DNA Prep Kit (Biofact, Daejeon, Korea)를 이용하여 genomic DNA를 추출하였다. 이후, internal transcribed spacer (ITS) 영역과 large subunit (LSU) rRNA 유전자의 증폭을 위해 각각 ITS1F/ITS4 및 LSU1Fd/LR5 primer를 사용하여 polymerase chain reaction (PCR)을 수행하였다[11–14]. 증폭된 PCR 산물은 ExoSAP-IT (Thermo Fisher Scientific, Waltham, MA, USA)를 처리하여 정제한 뒤, Macrogen (Daejeon, Korea)에 의뢰하여 염기서열 분석을 실시하였으며, 확보된 ITS 영역 및 LSU 유전자 염기서열은 NCBI (National Center for Biotechnology Information)와 KACC (Korean Agricultural Culture Collection)의 데이터베이스에 등록된 서열과 비교 분석하였다(Table 2). 계통학적 유연관계 분석은 MEGA 11.0 프로그램을 사용하여 Tamura-Nei 모델을 적용하였으며, 1,000회 반복한 bootstrap 분석을 바탕으로 maximum likelihood (ML) 계통수를 구축하였다[15–17].
Table 2. Accession numbers of sequences used for the phylogenetic analyses in this study
| Species name | Strain | Country | Genbank accession number | |
|---|---|---|---|---|
| ITS | LSU | |||
| Diplocarpon coronariae | CS01 | South Korea | AB494960 | AB494964 |
| Diplocarpon coronariae | GW01 | South Korea | AB494962 | – |
| Diplocarpon earlianum | CBS 162.32 | Unknown | MH855259 | MH866712 |
| Diplocarpon mespili | CBS 166.28 | England | – | MH877689 |
| Diplocarpon mespili | CBS 402.65 | China | – | MH870277 |
| Diplocarpon mespilicola | CF-2 | China | – | MW809414 |
| Diplocarpon mespilicola | CF-3 | China | – | MW809415 |
| Diplocarpon mespilicola | CGMCC3.20492 | China | – | MW809413 |
| Diplocarpon panattoniana | CBS 163.25 | Unknown | MH854831 | MH866332 |
| Diplocarpon rosae | 26L-434 | Mexico | AB609192 | – |
| Diplocarpon rosae | 26L-435 | Mexico | AY904059 | – |
| Diplocarpon rosae | CBS 163.31 | Unknown | MH855164 | MH866612 |
| Diplocarpon rosae | CBS 829.72 | Netherlands | – | MH872311 |
| Diplocarpon rosae | CFCC6814 | China | KP099199 | – |
| Diplocarpon rosae | DKU017 | South Korea | PP291862 | – |
| Diplocarpon rosae | DKU027 | South Korea | PP291868 | – |
| Diplocarpon rosae | DR-19 | Unknown | KP052773 | – |
| Diplocarpon rosae | NL1 | China | MW800033 | – |
| Diplocarpon rosae | RM071209004 | China | FJ493247 | – |
| Diplocarpon rosae | RM071209006 | China | FJ493242 | – |
| Diplocarpon rosae | RM080715007 | China | FJ493248 | – |
| Diplocarpon rosae | RM080715008 | China | FJ493249 | – |
| Diplocarpon rosae | TJ | China | PQ168924 | – |
| Diplocarpon rosae | UASWS0428 | Switzerland | HM235978 | – |
| Diplocarpon rosae | KNUF-24-AD | South Korea | PV270005 | PV270032 |
| Diplocarpon rosae | KNUF-24-CA | South Korea | PV270006 | PV270033 |
| Diplocarpon rosae | KNUF-24-ChJ | South Korea | PV270007 | PV270034 |
| Diplocarpon rosae | KNUF-24-CJ | South Korea | PV270008 | PV270035 |
| Diplocarpon rosae | KNUF-24-CW | South Korea | PV270009 | PV270036 |
| Diplocarpon rosae | KNUF-24-DG | South Korea | PV270010 | PV270037 |
| Diplocarpon rosae | KNUF-24-DJ | South Korea | PV270011 | PV270038 |
| Diplocarpon rosae | KNUF-24-DY | South Korea | PV270012 | PV270039 |
| Diplocarpon rosae | KNUF-24-GC | South Korea | PV270013 | PV270040 |
| Diplocarpon rosae | KNUF-24-GJ | South Korea | PV270014 | PV270041 |
| Diplocarpon rosae | KNUF-24-GM | South Korea | PV270015 | PV270042 |
| Diplocarpon rosae | KNUF-24-GN | South Korea | PV270016 | PV270043 |
| Diplocarpon rosae | KNUF-24-GoS | South Korea | PV270017 | PV270044 |
| Diplocarpon rosae | KNUF-24-GS | South Korea | PV270018 | PV270045 |
| Diplocarpon rosae | KNUF-24-HC | South Korea | PV270019 | PV270046 |
| Diplocarpon rosae | KNUF-24-HD | South Korea | PV270020 | PV270047 |
| Diplocarpon rosae | KNUF-24-JJ | South Korea | PV270021 | PV270048 |
| Diplocarpon rosae | KNUF-24-NW | South Korea | PV270022 | PV270049 |
| Diplocarpon rosae | KNUF-24-NYJ | South Korea | PV270023 | PV270050 |
| Diplocarpon rosae | KNUF-24-PC | South Korea | PV270024 | PV270051 |
| Diplocarpon rosae | KNUF-24-PH | South Korea | PV270025 | PV270052 |
| Diplocarpon rosae | KNUF-24-SC | South Korea | PV270026 | PV270053 |
| Diplocarpon rosae | KNUF-24-SJ | South Korea | PV270027 | PV270054 |
| Diplocarpon rosae | KNUF-24-SoC | South Korea | PV270028 | PV270055 |
| Diplocarpon rosae | KNUF-24-UJ | South Korea | PV270029 | PV270056 |
| Diplocarpon rosae | KNUF-24-US | South Korea | PV270030 | PV270057 |
| Diplocarpon rosae | KNUF-24-YD | South Korea | PV270031 | PV270058 |
| Marssonina brunnea | 14-4 | USA | MN315249 | – |
| Marssonina brunnea | 14-6 | USA | MN315250 | – |
| Marssonina balsamiferae | 14-19 | USA | MN315242 | – |
| Marssonina balsamiferae | 14-21 | USA | MN315243 | – |
| Pyrenophora lolii | CBS 240.48 | Netherlands | MH856325 | MH867879 |
ITS: Internal transcribed spacer regions; LSU: Partial sequence of large subunit rRNA gene.
Strains isolated in this study are indicated in bold.
장미 검은무늬병은 식재된 장미에서 주로 5월부터 11월까지 관찰되었으며, 감염 초기에는 잎에 병반이 형성된 후, 병이 진전되면서 조기 낙엽이 유도되었다(Fig. 2A). 채집한 장미 잎 시료에서 암갈색 또는 검은색의 반점이 관찰되었으며, 병반이 형성된 비정상 조직은 정상적으로 생육한 잎과 뚜렷한 차이를 보였다(Fig. 2A and B). 또한, 병징이 나타난 잎 표면에서는 미세한 검정색 돌기 구조가 관찰되었으며, 국내 27개 지역에서 채집한 총 22개 품종의 이병 시료를 비교 분석한 결과, 병징의 형태는 전반적으로 유사하였으며 품종 간 뚜렷한 증상의 차이는 관찰되지 않았다.
채집된 시료의 표면에 형성된 돌기를 실체현미경 및 광학현미경으로 관찰한 결과, 해당 구조는 분생자층(acervuli)으로 확인되었다(Fig. 2C). 분생자층의 내부에서는 다수의 분생포자형성세포(conidiogenous cells)가 관찰되었으며(Fig. 2D–F), 그 주변에서 다수의 분생포자(conidia)가 관찰되었다. 분생포자의 경우 투명한(hyaline) 타원형(ellipsoid) 또는 장타원형(oblong)으로, 1개의 격벽(1-septate)에 의해 2개의 세포로 구분되어 있었으며, 형태는 곧거나 약간 굽은 형태로 확인되었다. 분생포자의 크기는 16.5–25.8 × 4.7–6.5 µm (av. = 21.9 × 5.5 µm, n = 30)로 측정되었다(Fig. 2H). 배양학적 특징의 경우, 25°C에서 4주간 PDA 배지에서 균체를 배양하였을 때 암갈색 또는 어두운 올리브색의 균체가 형성되었다(Fig. 2G). 국내 27개 지역에서 분리된 27개 균주의 배양학적 및 형태적 특징을 비교한 결과, 모든 균주에서 유사한 특징이 확인되었다(Data not shown). 이에 본 연구에서는 전체 27개 균주 중 가장 먼저 분리된 KNUF-24-DG를 대표 균주로 선정하였다. 관찰된 배양학적 및 형태적 특징을 해외 기보고된 D. rosae의 특징과 비교한 결과, PDA 배지에서 형성되는 균총의 색은 모두 암갈색 또는 어두운 올리브색이었으며, 분생자층의 형태와 분생포자의 크기 및 형태 등 형태적 특징도 유사하였다(Table 3) [7,8].

Fig. 2. Symptoms observed on Rosa sp. and morphological characteristics of the Diplocarpon rosae KNUF-24-DG isolated from Daegu. (A and B): Black spot symptom on leaves; (C): Observed acervuli on symptomatic leaves; (D): Front and reverse view of colony on potato dextrose agar at 25°C for 28 days; (E–G): Conidiogenous cells with conidia; (H): Conidia. Scale bars: C = 1 mm; E = 20 μm; F–H = 10 μm.
Table 3. Comparison of morphological characteristics of Diplocarpon rosae KNUF-24-DG with reference species D. rosae
| Characteristics | Diplocarpon rosae KNUF-24-DGa |
D. rosaeb | D. rosaec | |
|---|---|---|---|---|
| Colony on PDA | Dark black to beige or dark olive |
N/A | Dark black to beige or dark olive |
|
| Conidiomata | Black, solitary | Black, solitary | Brown, solitary | |
| Conidiophore | Hyaline, straight or slightly curved |
N/A | N/A | |
| Conidia | Size (µm) | 16.5–25.8 × 4.7–6.5 | 14.0–22.5 × 5.0–7.5 | 18.0–25.0 × 5.0–6.0 |
| Shape | 2-celled, hyaline, straight or slightly curved |
2-celled, hyaline, straight or slightly curved |
2-celled, obovoid, holoblastic, straight or slightly curved |
|
aFungal strain used in this study; bSource of description [7]; cSource of description [8].
N/A: Data not available.
각 지역에서 분리된 27개 균주의 분자생물학적 동정을 위해 ITS 영역 및 LSU 유전자를 증폭한 결과, 각각 517 bp와 823 bp의 염기서열이 확보되었다. 확보된 ITS 영역 염기서열을 기반으로 상동성 분석을 수행한 결과, 해외에서 보고된 Diplocarpon rosae CBS 163.31, NL1, CFCC 6814 등의 균주 및 국내에서 등록된 D. rosae DKU027, DKU017, KACC 42437, KACC 40489 등과 지역에 상관없이 97.7–100%의 높은 염기서열 상동성을 보였다. 마찬가지로 LSU 유전자의 염기서열 상동성은 D. rosae CBS 163.31 및 CBS 829.72과 99.6–100%의 높은 염기서열 상동성이 확인되었으나, 국내 D. rosae 균주들의 경우 LSU 유전자 염기서열 정보가 등록되어 있지 않아 상동성 비교를 수행할 수 없었다. ITS 영역 염기서열을 기반으로 분자계통수를 작성하였을 때, 국내 D. rosae 균주들은 해외에서 기보고된 D. rosae 균주들과 함께 서로 다른 2개의 계통군으로 구분되었다. 대구, 남양주, 세종 지역에서 분리된 균주(KNUF-24-DG, KNUF-25-NYJ, KNUF-25-SJ)가 포함된 계통군의 경우 멕시코와 중국에서 보고된 D. rosae 균주 및 국내에서 등록된 D. rosae KACC 40489와 동일한 계통군이 형성되었으며, 합천, 대전, 천안 지역에서 분리된 균주(KNUF-25-HC, KNUF-25-DJ, KNUF-25-CA)가 포함된 다른 계통군에서는 중국에서 보고된 D. rosae CFCC 6814 및 국내에서 등록된 D. rosae DKU017, DKU027, KACC 42437과 동일한 계통군이 형성되었다(Fig. 3). LSU 유전자 염기서열을 기반으로 분자계통수를 작성하였을 때 역시 서로 다른 2개의 계통군으로 나뉘어지는 것이 확인되었으며, 해외에서 기보고된 D. rosae CBS 163.31 및 CBS 829.72 균주가 각각 구분되었다(Fig. 4). 또한 ITS 영역과 LSU 유전자 염기서열을 종합하여 작성된 분자계통수에서 두 계통군으로 구분되었으며, D. rosae CBS 163.31과 동일한 계통군이 형성되었다(Fig. 5). 본 연구에서 분리한 27개 장미검은무늬병균의 배양학적 및 형태적 특징은 기존에 보고된 D. rosae의 균학적 특징과 유사하였으며, 분자생물학적 분석 결과에서도 모든 균주가 기보고된 D. rosae 균주와 동일한 계통군을 형성하였다. 이에 따라 국내 27개 지역에서 발생한 장미검은무늬병의 원인균은 모두 D. rosae로 동정되었다.
Diplocarpon 속은 1912년 미국의 식물병리학자 Wolf에 의해 처음 보고되었으며, 사과나무, 딸기, 장미 등 다양한 기주 식물에 병을 일으키는 식물병원균으로 알려져 있다[5,18,19]. Diplocarpon 속에는 현재 전 세계에 총 9종이 보고되어 있으며, 국내의 경우 D. coronariae, D. fragariae, D. rosae 3종이 보고되어 있다[20,21]. 그 중 D. rosae는 장미(Rosa spp.)에 장미 검은무늬병을 일으키는 병원균으로 빗물과 바람, 그리고 관수 시 비산하는 물방울 등을 통해 식물체로 전반되며, 이러한 특성으로 인해 장미가 식재된 시설 내에서 반복적으로 많은 피해를 일으키고 있다[6]. 2022년 국립산림과학원이 발표한 생활권 수목 피해 진단 보고서에 따르면, 2021년 한 해 동안 장미 검은무늬병은 총 56종의 병해 중 8번째로 많이 접수된 병해로 보고되었으며, 163종의 피해 접수 수종 중에서도 8위를 기록하는 등 특히 장미가 조경수로 활용되는 공원 및 시설 화단 등에서 매년 지속적인 피해가 발생하는 것으로 알려져 있다[22]. 장미 검은무늬병의 병원균인 D. rosae의 형태적 특징은 1912년 Wolf에 의해 병반의 형태와 크기, 분생자층 및 분생포자의 구조와 색상 등을 중심으로 처음 보고되었으며, 이후 배양학적 특징은 1948년 Baker에 의해 PDA 배지에서의 느린 생장속도로 기술되었다[8]. 국내에서는 2000년 서울, 춘천, 부산, 강릉 등 다양한 지역에서 채집된 D. rosae 균주의 분생자층, 분생포자형성세포 및 분생포자의 형태, 색상, 크기 등 형태적 특징이 보고된 바 있다[7]. 그러나 현재까지 국내에서 분리된 D. rosae 균주의 배양학적 특징에 대한 보고는 없으며, 본 연구에서 제시한 국내 분리 균주의 배양학적 특성은 향후 관련 연구를 위한 기초 자료로 활용될 수 있을 것으로 기대된다.
추가적으로, 최근 해외에서 D. rosae의 유전체 및 전사체 분석 연구가 활발히 이루어지고 있으나, 분리 지역 및 국가 간 D. rosae 균주의 균학적 특징 및 계통학적 유연관계를 종합적으로 비교한 연구는 아직 제한적인 실정이다[23,24]. 특히 현재 NCBI와 KACC에 등록된 D. rosae의 염기서열 정보는 대부분 ITS 영역에 국한되어 있어, 균주 간 계통학적 유연관계를 정밀하게 분석하는 데 한계가 있다. 따라서 향후 다양한 지역 및 국가에서 분리된 장미 검은무늬병 균주의 유전 정보를 폭넓게 확보하고, ITS 영역 이외의 다양한 분자마커를 활용한 분자생물학적 분석을 통해 D. rosae의 균주 간 계통학적 유연관계를 정밀하게 규명할 필요가 있다. 이러한 분석을 바탕으로 계통군 간 병원성 및 생물학적 특성 차이를 비교 및 분석함으로써, 장미 검은무늬병의 효과적인 방제 전략 수립을 위한 기초 자료로 활용될 수 있을 것으로 판단된다.

Fig. 3. Maximum likelihood phylogenetic tree based on ITS regions sequence showing the phylogenetic position of the isolated strains among the related strains in the genus Diplocarpon. Pyrenophora lolli CBS 240.48 was used as the outgroup. The strains isolated in this study are indicated in bold, and the numbers above the branches represent the bootstrap values (> 60%) obtained for 1,000 replicates. Scale bar = 0.050 substitutions per nucleotide position.
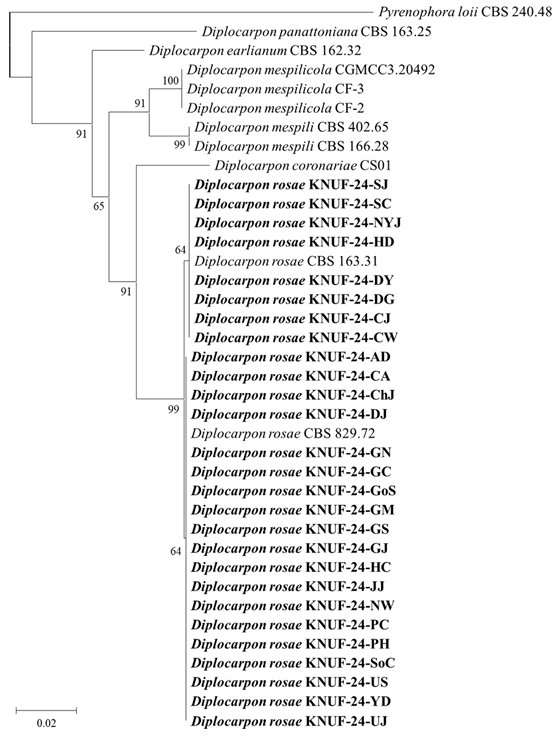
Fig. 4. Maximum likelihood phylogenetic tree based on LSU gene sequence showing the phylogenetic position of the isolated strains among the related strains in the genus Diplocarpon. Pyrenophora lolli CBS 240.48 was used as the outgroup. The strains isolated in this study are indicated in bold, and the numbers above the branches represent the bootstrap values (> 60%) obtained for 1,000 replicates. Scale bar = 0.02 substitutions per nucleotide position.

Fig. 5. Maximum likelihood phylogenetic tree based on ITS regions and LSU gene sequences showing the phylogenetic position of the isolated strains among the related strains in the genus Diplocarpon. Pyrenophora lolli CBS 240.48 was used as the outgroup. The strains isolated in this study are indicated in bold, and the numbers above the branches represent the bootstrap values (> 60%) obtained for 1,000 replicates. Scale bar = 0.050 substitutions per nucleotide position.
본 결과물은 농림축산식품부의 재원으로 농림식품기술기획평가원의 농식품기술융합창의인재양성 사업의 지원을 받아 연구되었음(no.321001-03).
The authors declared no potential conflicts of interest.
Kumar N, Srivastava GC, Dixit K. Flower bud opening and senescence in roses (Rosa hybrida L.). Plant Growth Regul 2008;55:81–99. https://doi.org/10.1007/s10725-008-9263-x
Ministry of Agriculture, Food and Rural Affairs. 2022 status of flower crop cultivation in Korea [Internet]. Sejong: Korea Agricultural Statistics Service; 2022 [cited 2025 Dec 23]. Available from: https://kass.mafra.go.kr
Yoon SH, Hong SB, Choi YJ, Lee DH, Lee SY, Choi HY, et al. List of plant diseases in Korea. 6th ed. Seoul: The Korean Society of Plant Pathology; 2023. p. 420–1.
Blechert O, Debener T. Morphological characterization of the interaction between Diplocarpon rosae and various rose species. Plant Pathol 2005;54:82–90. https://doi.org/10.1111/j.1365-3059.2005.01118.x
Wolf FA. The perfect stage of Actinonema rosae. Bot Gaz 1912;54:218–34.
Gachomo EW, Kotchoni SO. Detailed description of developmental growth stages of Diplocarpon rosae in Rosa: A core building block for efficient disease management. Ann Appl Biol 2007;151:233–7. https://doi.org/10.1111/j.1744-7348.2007.00167.x
Lee HT, Shin HD. Taxonomic studies on the genus Marssonina in Korea. Mycobiology 2000;28:39–46. https://doi.org/10.1080/12298093.2000.12015720
Baker KF. The history, distribution, and nomenclature of the rose black-spot fungus. Plant Dis Rep 1948;32:260–74.
Lee DH, Back CG, Win NKK, Choi KH, Kim KM, Kang IK, et al. Biological characterization of Marssonina coronaria associated with apple blotch disease. Mycobiology 2011;39:200–5. https://doi.org/10.5941/myco.2011.39.3.200
Whitaker VM, Hokanson SC, Bradeen J. Distribution of rose black spot (Diplocarpon rosae) genetic diversity in Eastern North America using amplified fragment length polymorphism and implications for resistance screening. J Amer Soc Hort Sci 2007;132:534–40. https://doi.org/10.21273/JASHS.132.4.534
Gardes M, Bruns TD. ITS primers with enhanced specificity for basidiomycetes-application to the identification of mycorrhizae and rusts. Mol Ecol 1993;2:113–8. https://doi.org/10.1111/j.1365-294x.1993.tb00005.x
White TJ, Bruns TD, Lee SB, Taylor JW. Amplification and direct sequencing of fungal ribosomal RNA genes for phylogenetics. In: Innis MA, Gelfand DH, Sninsky JJ, White TJ, editors. PCR protocols: A guide to methods and applications. San Diego: Academic Press; 1990. p. 315–22. https://doi.org/10.1016/B978-0-12-372180-8.50042-1
Crous PW, Schoch CL, Hyde KD, Wood AR, Gueidan C, de Hoog GS, et al. Phylogenetic lineages in the Capnodiales. Stud Mycol 2009;64:17–47. https://doi.org/10.3114/sim.2009.64.02
Vilgalys R, Hester M. Rapid genetic identification and mapping of enzymatically amplified ribosomal DNA from several Cryptococcus species. J Bacteriol 1990;171:4238–46. https://doi.org/10.1128/jb.172.8.4238-4246.1990
Tamura K, Stecher G, Kumar S. MEGA11: Molecular evolutionary genetics analysis version 11. Mol Biol Evol 2021;38:3022–7. https://doi.org/10.1093/molbev/msab120
Tamura K, Nei M. Estimation of the number of nucleotide substitutions in the control region of mitochondrial DNA in humans and chimpanzees. Mol Biol Evol 1993;10:512–26. https://doi.org/10.1093/oxfordjournals.molbev.a040023
Felsenstein J. Evolutionary trees from DNA sequences: A maximum likelihood approach. J Mol Evol 1981;17:368–76. https://doi.org/10.1007/bf01734359
Dumont B, Schmitz S, Mulot E, Ghesquiere A, Chandelier A, Lateur M. First report of Diplocarpon coronariae causing apple blotch disease of apple tree in Belgium. New Dis Rep 2024;50:e70003. https://doi.org/10.1002/ndr2.70003
Chandel S, Chauhan P, Panwar R. Occurrence of black spot of rose, Marssonina rosae from Himachal Pradesh, India. Int J Curr Microbiol App Sci 2017;6:3058–60. https://doi.org/10.20546/ijcmas.2017.608.365
International Mycological Association, Westerdijk Fungal Biodiversity Institute. MycoBank [Internet]. Utrecht: International Mycological Association, Westerdijk Fungal Biodiversity Institute; 2026 [cited 2026 Jan 9]. Available from: https://www.mycobank.org
National Institute of Biological Resources (NIBR). National species list of Korea 2024 [Internet]. Incheon: NIBR; 2024 [cited 2026 Jan 9]. Available from: https://species.nibr.go.kr
National Institute of Forest Science (NIFoS). Analysis report of private consulting prescriptions for urban tree healthcare in 2021 [Internet]. Seoul: NIFoS; 2022 [cited 2026 Jan 9]. Available from: http://book.nifos.go.kr
Neu E, Featherston J, Rees J, Debener T. A draft genome sequence of the rose black spot fungus Diplocarpon rosae reveals a high degree of genome duplication. PLoS One 2017;12:e0185310. https://doi.org/10.1371/journal.pone.0185310
Neu E, Debener T. Prediction of the Diplocarpon rosae secretome reveals candidate genes for effectors and virulence factors. Fungal Biol 2019;123:231–9. https://doi.org/10.1016/j.funbio.2018.12.003