서론
우리나라의 2016년 버섯 생산량은 186,306톤으로 표고, 느타리, 큰느타리, 팽이, 양송이 등이 1만톤 이상 생산하는 주요 품목이다[1, 2]. 우리의 주변국인 중국[3]과 일본[4]은 생산량뿐만 아니라 품목의 종류에서도 우리보다 훨씬 다양하다. 따라서 우리나라는 다양한 품목개발과 경쟁력 있는 품목의 대량생산 체계를 구축할 필요가 있다.
품목 다양성 측면에서 우리나라는 가을철 강원도를 중심으로 느타리와 매우 비슷한 ‘참부채버섯’이라는 버섯을 채취하여 식용하고 있다. 이 버섯은 식용 및 약용으로 쓰이며, 추출물에 의한 항암 활성[5]과 YAC-1 세포에서 세포독성 활성[6]도 나타내고 있다. 또한 참부채버섯은 면역력을 조절하고 혈중지질 농도를 낮추며 바이러스 작용을 억제하는 기능도 밝혀졌다[7].
참부채버섯은 동남아시아에서 흔히 볼 수 있는 식용버섯 중 하나지만 우리나라에서는 아직 인공재배가 되고 있지 않다. 우리나라와 인접한 중국과 일본도 이 버섯에 대해 관심은 있으나, 상업적인 재배가 아직 이루어지고 있지는 않다. 한편, 국립산림과학원은 2010년부터 국내 버섯자원을 체계적으로 수집하면서 야생버섯의 기초특성을 조사하고 있다[8, 9].
참부채버섯의 인공재배에 관한 연구는 미흡한 실정이고 국내 보급을 위해서는 균사배양 특성 및 적정 재배 환경을 구명하고 우량균주를 선발하는 연구가 시급한 실정이다. 본 연구에서는 국내에서 참부채버섯이라고 하여 수집한 버섯자원에 대해 Ribosomal DNA중에서 5.8S를 포함하는 internal transcribed spacer (ITS) 부위의 염기서열을 이용하여 계통수 분석을 실시하였으며, 수집 균주 사이의 유연관계를 파악하였다. 버섯재배를 위한 기초특성을 파악하기 위해 균사배양 특성 및 재배시험을 실시하였다.
재료 및 방법
시험 균주
본 시험에 사용된 균주는 국립산림과학원(National Institute of Forest Science, NIFoS)에 보관 중인 것을 사용하였다. 사용 균주는 강원도 평창군 중왕산과 가리왕산에서 수집한 6개 균주, 경기도 구리시 동구릉에서 수집한 1개 균주와 가평군 화악산에서 수집한 1개 균주이다(Table 1, Fig. 1). 균주는 4℃ 보관실에 보관 중이던 균을 감자한천 배지(potato dextrose agar, PDA)에 이식한 후 직경이 3 cm 이상 자랐을 때 균총의 가장 자리에서 직경 8 mm의 cork borer로 떼어 새로운 배지에 이식하였다. 균이 접종된 배지를 암 상태의 25℃ 항온기에서 20일간 배양 후 본 시험에 사용하였다.
Genomic DNA 분리, ITS PCR 증폭 및 염기서열 분석
배양된 균사체를 동결건조 후 유발에 넣고 액체질소를 첨가하여 곱게 마쇄하였다. DNA는 DNeasy plant mini kit (Qiagen, Germantown, MD, USA)를 이용하여 추출하였다. 흡광도 (optical density, O.D.)를 측정해서 template DNA 농도를 조정하였다. 본 연구에서 rDNA ITS 영역을 분리하기 위하여 28S rDNA의 5’말단과 18S rDNA의3’말단을 포함하는 ITS 1, ITS 4 primer를 이용하였다[10]. PCR 증폭은 Accuprep PCR Premix kit(Bioneer, Daejeon, Korea)를 이용하였으며, Bio-Rad T100 Thermal Cycler (Bio-Rad, Hercules, CA, USA)를 이용하여 실시하였다. PCR 반응조건은 template predenaturation는 94℃에서 5분간 반응 후 denaturation는 94℃에서 1분, annealing은 56℃에서 1분, extension은 72℃에서 2분을 1 cycle로 하여, 총 35 cycle을 돌린 후 PCR 산물을 4℃에 보관하여 다음 시험에 사용하였다. PCR 산물을 1.5%의 agarose gel에서 전기영동 하였고 Dyne LoadingSTAR (DYNEBIO, Seongnam, Korea)로 염색하여 UV illuminator 위에서 band를 확인하였다. 증폭된 DNA는 마크로젠(Macrogen, Seoul, Korea)에 의뢰하여 염기서열 분석을 실시하였다.
계통수 분석
결정된 염기서열은 미국생물정보센터(National Center for Biotechnology Information, NCBI, http://www.ncbi.nlm.nih.gov)에서 BLAST 프로그램을 사용하여 GenBank DNA 데이터베이스에 등록되어 있는 균류의 ITS 염기서열과 상동성을 비교하였다. NCBI의 GenBank에서 확인된 관련된 균류의 염기서열을 이용하여 MEGA X [11, 12]로 계통수 분석을 실시하였다. 이를 위해 neighbor-joining 방법[13]을 이용하였으며, 계통도 가지의 clade 신뢰도는 1,000번의 bootstrap resampling을 수행하여 평가하였다.
Universal Fungal PCR Fingerprinting (UFPF)에 의한 균주 간 유연관계 분석
균주 간 유연관계를 분석하기 위하여 Universal Fungal PCR Fingerprinting kit (BioTech. Ltd) 를 이용하였다. 증폭 조건은, template predenaturation는 94℃에서 5분간, denaturation는 94℃에서 1분, annealing은 55℃에서 1분, extension은 72℃에서 2분간 35 cycle 한 후 72℃에서 7분간 반응시켰다. UFPF primer kit의 sequence를 이용한 PCR 결과 12개의 다형성을 보이는 band가 있으면 1, 없으면 0으로 구분하여 SIMQULA의 계수를 계산 하였고, 이 계수를 이용하여 MEGA X 프로그램의 UPGMA (Unweighted par-Group method with Arithmetic means)로 군(cluter) 분석하였다[11, 12].
배지 종류별 균사생장
사용 배지는 potato dextrose agar (PDA; Difco, Detroit, MI, USA), malt extract agar (MEA; Difco), Sabouraud dextrose agar (SDA; Difco)를 사용하였다. 배지는 고압살균(121℃, 1.2 kgf/cm2, 20분) 후 무균상에서 petridish (bottom 85 mm × height 15 mm)에 20 mL를 분주하여 완전히 식힌 후 사용하였으며, 3반복으로 균을 접종하여 25℃에서 21일간 암배양 후 균사생장을 조사하였다[8].
온도별 균사생장
균주의 균사생장에 적합한 최적 온도를 구명하기 위하여 20분간 고압살균(121℃, 1.2 kgf/cm2) 된 선발 배지를 petri-dish에 20 mL씩 분주하여 고체화시킨 평판배지에 접종원을 직경 8 mm인 cork borer로 절취하여 3반복 접종하고 배양온도가 각각 10℃, 15℃, 20℃, 25℃, 30℃로 조절된 항온기에서 21일간 암배양 후 균총의 직경을 조사하였다[8].
pH별 균사생장
균주의 배양에 적합한 최적 pH를 알아보기 위하여 액체배지(potato dextrose broth, PDB; Difco)에 0.1 N HCI, NaOH를 이용하여 pH가 4.0, 5.0, 6.0, 7.0, 및 8.0가 되도록 조제하였으며, 100 mL 삼각플라스크에 20 mL씩 분주하여 20분간 고압살균(121℃, 1.2 kgf/cm2) 후 실온에서 냉각시킨 다음 접종원(ø⌀8 mm)을 접종하고, 25℃ 항온기에서 21일간 암배양 후 균사체량을 측량하였다. 균체량은 배양액을 여과지(No.2; Whatman, Piscataway, NJ, USA)로 균사를 분리하여 건조(70℃, 2 days) 후 건중량(mg/flask)을 측량하였다[8].
버섯 균주의 CM-cellulase 활성 조사
섬유소 분해효소 cellulase의 활성을 조사하기 위해 Kasana 등[14]의 방법에 따라 carboxymethylcellulose (CMC) 1 L를 NaNO3 2 g, K2HPO4 1 g, MgSO4 0.5 g, KCl 0.5 g, carboxymethylcellulose sodium salt 2 g, peptone 0.2 g, agar 15 g을 첨가하여 pH 6.0으로 조성한 후 10 mL씩 분주하여 사용하였다. CMC 배지에 공시균을 접종(ø⌀6 mm)한 후, 25℃에서 8일간 암배양 후 cellulase 활성을 측정하였다. cellulase 활성은 배지의 중앙에 염색시약인 Gram’s iodine solution (KI 2 g, I2 1 g, 증류수 300 mL)을 1~2 mL씩 첨가한 후에 25℃에서 이루어졌으며, 배지 내 cellulase 비활성 영역과 활성 영역 중 투명대의 직경을 mm 단위로 측정하여 기록하였다[8].
버섯 균주의 laccase 활성 조사
리그닌 분해효소 중 하나인 laccase 활성을 조사하기 위해 Crowe과 Olsson [15]이 식물 병원성 토양 진균의 laccase 활성을 검색하기 위해 사용했던 방법을 사용하였다. 무기물 혼합 농축액(K2HPO4 2 g, KCI 2g, MgSO4•7H2O 2g, D.W. 1L, pH 5.0) 50 mL와 2, 2'-azino-bis(3-ethylbenzthiazoline-6-sulfonic acid) (ABTS) 0.5487 g을 첨가하여 혼합액의 최종 부피가 1 L가 되도록 하였다. 혼합액에 한천(Bacto agar; Difco) 15 g을 첨가한 것을 20 mL씩 분주하여 고압살균(121℃, 1.2 kgf/cm2, 20분) 후 사용하였다. laccase 활성은 완성된 배지에 공시균을 1개씩 접종(ø 8 mm)한 후, 25℃에서 5일간 암배양하여 관찰하였고, 접종원을 중심으로 청록색의 원형 발색대의 크기를 mm 단위로 측정하여 기록하였다[8].
톱밥배지 수종선발
배지별 균주를 선발하기 위하여 균주별로 톱밥배지에 균사생장속도를 조사하였다. 시험관 배지는 시험관 칼럼(200 × 30 mm)에 신갈나무(Quercus mongolica), 상수리나무(Q. acutissima), 자작나무(Betula platyphylla var. japonica), 잣나무(Pinus koraiensis), 소나무(P. densiflora), 미루나무(Populus deltoides) 등을 사용하였으며, 톱밥은 10~20 mesh 체로 친 후, 배지의 수분을 65%로 조절하였다. 수분이 조제된 배지는 용적밀도가 0.21 kg/cm2이 되도록 충전하여 90분간 고압살균(121℃)한 후 실온으로 냉각된 배지를 무균상 내에서 균을 접종하였다. 접종 된 배지는 23℃로 조절된 배양실에서 50일간 배양하며 균사생장을 측정 하였으며 균사밀도를 육안으로 조사하였다.
톱밥 배지를 이용한 버섯 재배
버섯 톱밥재배에는 신갈나무 톱밥(Q. mongolica) 40%, 상수리나무 톱밥(Q. acutissima) 40%, 미강(rice bran) 20%를 재료로 하여 혼합하였고 수분함량은 65%로 맞춘 사각배지(2 kg)를 이용하였다. 제작한 배지는 121℃에서 90분간 고압살균 하여 이용하였다. 종균 접종 후 균 배양 관리는 배지온도 23℃에서 80~85일간 배양하고 이를 접종원으로 사각배지에서 균배양이 완료된 후 자실체 발생을 실시하였다.
자실체 발생 조건은 습도 85%, 실내온도 17~18℃, 광 80~120 lux 정도로 유지하여 관리하였다. 자실체의 크기와 모양이 좋고, 단단하며 상품성을 가질 수 있는 수확 적기를 조사하기 위하여 인공재배 된 균주의 자실체를 생육 단계별 크기와 갓과 대를 측정하였다.
결과 및 고찰
ITS 염기서열에 의한 종속간 유연관계 분석
ITS 영역의 염기서열을 이용하여 BLAST search를 통하여 기존에 알려진 균류의 염기서열들과 비교 분석하였다. 그 결과 Panellus edulis AB819092 염기서열과 99%의 상동성을 나타내었다. 분석한 ITS 영역 염기서열은 NCBI의 GenBank DNA database에 등록하였고 accession 번호는 MH747085~MH747092이며 Table 1에 제시하였다.
계통수 분석은 MEGA version X [11, 12]를 이용하여 neighbor-joining 방법으로 실시하였다(Fig. 2). 그 결과 본 실험에 이용한 균주들은 기존에 Panellus edulis로 명명된 염기서열과 단계통을 이루는 것을 확인하였다. 이 종은 2003년 중국에서 어떤 종의 갓이 황색 유형과 녹색 유형으로 나누면서 새롭게 명명된 것이다[16, 17]. 국내에서 참부채버섯이라고 알려진 종은 Panellus serotinus이나 본 연구에서는 확인하지 못하였으며, 이를 확인하기 위해 추후 더 광범위한 지역에서 수집한 시료를 이용한 연구가 필요하다.
UFPF 다형성 속간 유연관계 분석
UFPF PCR 분석을 위해 국내 수집 균주 8개를 비교하여 유연관계를 관찰하였다. UPGMA방법으로, 유연관계 분석은 radiation에 정확성을 알기 위해 3번 반복하였다(Fig. 3). NIFoS 2264, 2387, 2804, 2805, 3993가 한 그룹(Group I)으로 묶였으며, NIFoS 2407, 2792, 2803가 다른 한 그룹(Group Ⅱ)으로 묶였다. 평창에서 수집한 균주들은 Group I과 Group Ⅱ에 고르게 분포하는 것을 확인하였으며, 가평에서 수집한 균주(NIFoS 3993)는 Group I에 묶였지만 평창에서 수집한 균주들과 따로 떨어져 있는 모습을 나타내었으며, 구리에서 수집한 균주(NIFoS 2792)는 평창에서 수집한 균주와 그룹을 형성하였다. 품종 개발은 다양한 변이를 지닌 균주를 요구하기 때문에 보유하고 있는 유전자원에서 상업적으로 사용되는 품종의 분류가 더욱 중요하다[18]. 위 실험 내용을 근거로 국내 P. edulis의 야생 수집 균주를 인공재배하여 이를 토대로 추후에 우수한 품종으로 활용될 것이라 기대된다.
배지 종류별 균사생장
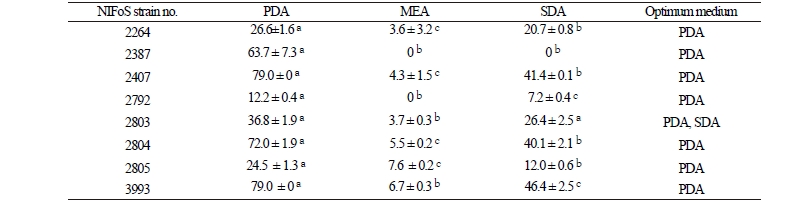
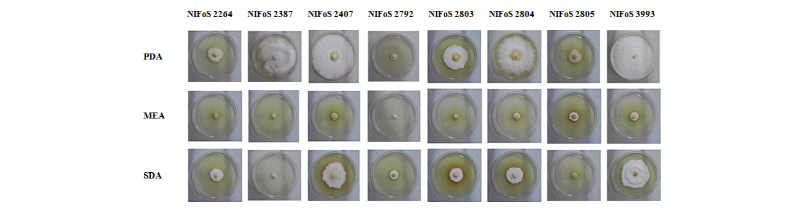
8개의 P. edulis 균주는 모두 PDA 배지에서 균사생장이 가장 좋았으며 다음으로 SDA 배지였고, MEA 배지에서 생장이 가장 저조하였다(Table 2, Fig. 4), PDA 배지에서는 NIFoS 2407, 3993 균주의 균사생장속도가 가장 빠른 것으로 나타났고 SDA 배지에서도 같은 결과로 나타났다.
온도별 균사생장
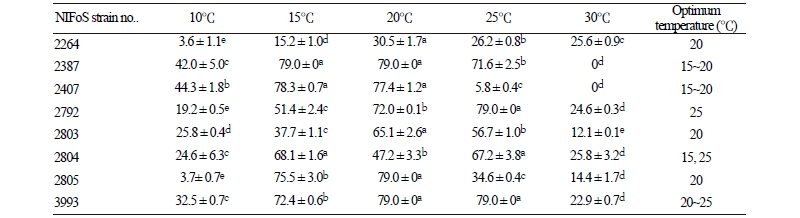
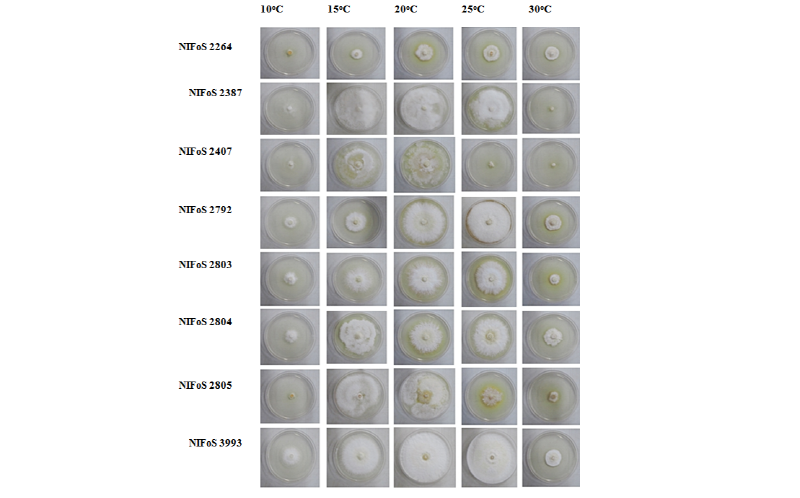
대부분 균주에서는 10℃ 저온성과 30℃ 고온성에서 균사 생장력이 낮은 것으로 조사되었다(Table 3, Fig. 5). 버섯 균들은 저온, 고온 환경에 대한 적응력이 많이 떨어지는 것을 알 수 있었다. NIFoS 2264 균주는 온도에 상관 없이 모두 균사생장이 저조하였다. 또한 NIFoS 2407, 2805의 경우에는 균총의 가장자리가 불규칙한 형태를 이루며 균사가 생장하는 특성이 관찰되었다. NIFoS 2387에서 최적온도 범위는 15~20℃였고, NIFoS 3993의 최적온도 범위는 20~25℃ 이었다. P. edulis의 온도별 균사생장은 15~25℃에서 양호하였으며, 그 중 25℃에서 균총의 크기가 가장 크게 나타나 균이 생장하기에 최적 온도임을 알 수 있었다. 이 버섯은 늦은 가을에 발생하는 버섯으로 생태적인 영향을 반영한 결과로 생각된다[8].
pH별 균사생장
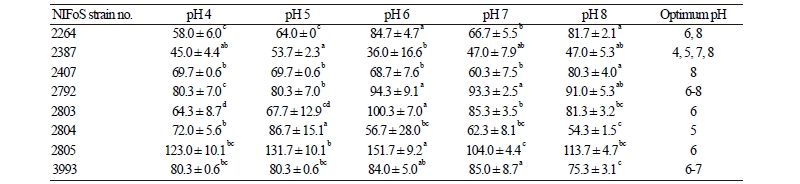
배양 21일 후 PDB 액체배지의 pH에 따른 균사량을 조사한 결과(Table 4) 생장 및 밀도를 고려하면 pH 6.0이 배지의 최적 산도로 조사 되었다. 이러한 균사 특징은 조사한 8균주중 5균주에서 두드러지며, 시험균의 pH 6.0인 배지에서 가장 많은 균사체량을 생산한 균주는 NIFoS 2805로, 151.7 mg/flask로 나타났다. 그중 가장 뚜렷한 것은 NIFoS 2804는 pH 5.0에서, NIFoS 2803, 2805는 pH 6.0로 나타났다. 예외적으로 NIFoS 2407은 pH 8.0에서, NIFoS 2264, 2387, 3993는 pH에 균체량에 영향을 받지 않았다.
pH 6.0값의 배지에서 상당히 잘 자라는 균들이 같은 농도에서 세포외 다당체 및 균체의 생산도 높다는 것이 보고되었다[19].
버섯 균주의 cellulase 활성
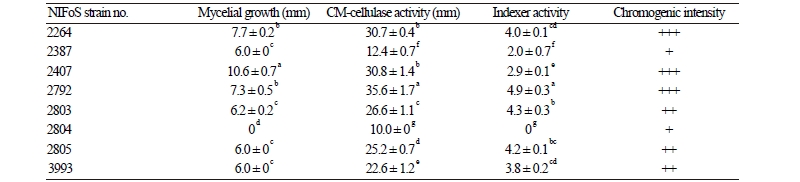
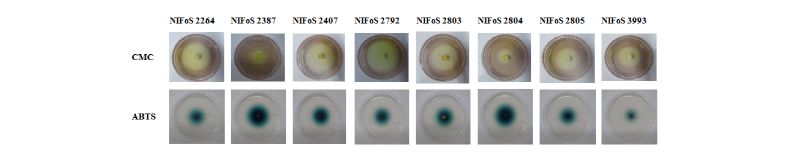
버섯의 셀룰라아제(cellulase)는 섬유소를 당(sugar)으로 가수분해하는 반응을 촉매하는 효소로[14], Carboxymethylcellulose (CMC)는 미생물에 의해 빨리 가수분해 된다. Cellulase 생산 균주를 검색하는데 유용하게 사용되기 때문에[20] 상업적인 측면에서 높은 활용 가치를 갖고 있다. 이와 같은 CMC agar plate에서 균을 접종하고 25℃에서 8일간 배양하여 조사하였다(Table 5, Fig. 6).
CM-cellulase 활성은 균주 중 NIFoS 2264, 2407, 2792에서 발색대의 크기가 30 mm 이상, 발색 강도가 strong (+++)으로 다른 균주들에 비해 높게 나타났다. 반면 NIFoS 2387, 2804에서는 13 mm 이하, 발색 강도가 weak (+)로 비교적 낮은 효소 활성이 나타났다. 이는 CMC agar plate 상에서는 CM-cellulase 활성과 균사생장과 같은 비례적인 관계에 있지 않을 수도 있다는 것을 제시하였다[8]. 또한 여기에서 사용한 cellulase 활성 검색법은 균주 간 cellulase 활성을 수치적으로 비교할 수 있었고, 무엇보다 여러 종류의 버섯 균주를 대상으로 cellulase 생산 유무를 판별해야 하는 경우에는 간편하고 유용한 방법이 될 수 있다.
버섯 균주의 laccase 활성
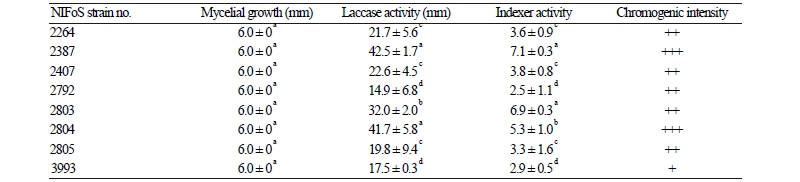
P. edulis의 리그닌 분해력을 조사하기 위해 ABTS agar plate 상에 laccase 활성을 조사하고, 균을 접종하여 25℃에서 5일간 배양하였다(Table 6, Fig. 6). 이 실험에서 NIFoS 2387, 2804는 laccase 활성의 발색대의 크기가 40 mm 이상, 발색 강도가 strong (+++)로 높은 활성을 나타났다. NIFoS 3993은 발색대의 크기가 18 mm 이상, 발색 강도가 weak (+)로 나타나 비교적 낮은 활성을 보였고, 나머지 균주들은 laccase 활성의 발색 강도는 moderate (++)로 활성을 보였다.
Cellulase 활성이 높은 균주는 NIFoS 2264, 2407, 2792와 활성이 낮은 균주는 NIFoS 2387, 2804로 확인되었는데, 이 결과는 laccase 활성이 높은 균주와는 반대의 결과를 얻었다. Cellulase의 활성이 높은 균주가 laccase 활성이 높은 것으로 보고되기도 하였으나[8], P. edulis는 그렇지 않아 균주의 분해효소들의 작용 기작에 대해 더 연구할 필요가 있었다.
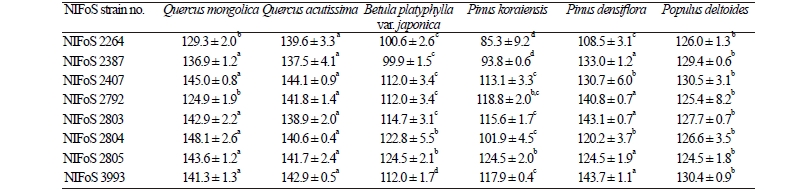
톱밥배지 수종 선발
톱밥배지 시험관에서 수종별로 50일간 균사생장 속도를 조사한 결과, NIFoS 2804균주는 신갈나무 톱밥에서 148.1 ± 2.6 mm/50 day이며 가장 균사 속도가 양호하였고 다른 톱밥 종류에서도 124.5 mm/50 day 이상으로 균사의 생장형태가 균일하였다. NIFoS 3993균주는 소나무 톱밥배지의 평균 균사생장은 143.7 ± 1.1 mm/50 day로 균사생장이 가장 높았다. 그 반면 균사배양 시 NIFoS 2387의 형태상으로는 균사의 생장 형태가 불규칙하고 톱밥 배지에서도 생장이 늦은 것이 많았다. 시험관 내 미루나무 톱밥은 빠르게 생장하였지만 균사밀도가 낮은 것을 알 수 있었다. P. edulis 버섯 인공재배를 위한 적정 배지 재료로 대체적으로 모든 균주에서 높은 생장량을 보인 상수리나무와 신갈나무 톱밥을 선발하였다(Table 7).
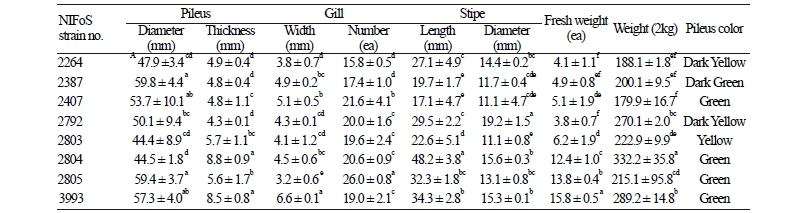
자실체 특성 및 우수 균주 선발
P. edulis 우수 균주를 선발하기 위하여 신갈나무 톱밥(Q. mongolica) 40%, 상수리나무 톱밥(Q. acutissima) 40%, 미강(Rice bran) 20%를 재료로 하여 2 kg 사각형 배지를 제작하고 균주를 접종하였다. 균사배양 적온은 23℃이며 배양기간은 접종 후 80~85일이 소요되었다. 원기형성은 10~11일이 소요되었고 수확까지의 자실체 생육기간은 17~18℃에서 각각 15~20일 소요되었다. 사각배지에서 8개 균주를 재배하여 수량을 조사한 결과(Table 8) 버섯의 색깔 및 버섯 형태에 차이가 있음을 확인할 수 있었다(Fig. 7). P. edulis는 갓색이 노랑색과 녹색으로 구분되어 있고[17], 자실체 주요 특성에서 갓색이 녹색인 NIFoS 2804는 갓직경 44.5 ± 1.8 mm, 갓두께 8.8 ± 0.9 mm, 대길이 48.2 ± 3.8 mm, 대두께 15.6 ± 0.3 mm, 무게 332.2 ± 35.8 g 이었고, 그 다음에는 갓색이 녹색인 NIFoS 3993에서 무게 289.2 ± 14.8 g로 두 번째로 수량이 높았다. 노랑색인 NIFoS 2792는 갓직경 50.1 ± 9.4 mm, 갓두께 4.3 ± 0.1 mm, 대길이 29.5 ± 2.2 mm, 대두께 19.2 ± 1.5 mm, 무게 270.1 ± 2.0 g이었다. 이와 같이 재배적 특성 및 품질을 고려하였을 때 갓색이 녹색인 NIFoS 2804, 3993균주와 노랑색인 NIFoS 2792는 우수한 특성을 나타내었다(Table 2, Table 8).
적요
국내에서 참부채버섯(Panellus serotinus)으로 수집한 8균주의 internal transcribed spacer 영역 염기서열을 이용하여 계통분석을 실시한 결과 참부채버섯이 아닌 Panellus edulis로 나타났다. Universal Fungal PCR Fingerprinting (UFPF) 분석결과 P. edulis 8균주는 크게 두 그룹으로 나눠졌다. 우리나라 산림에 서식하는 8개 균주의 배양특성을 이해하기 위해 균사의 성장과 효소 활성에 대한 기초특성 연구를 수행했다. 모든 균주는 21일 동안 3종류 배지를 사용하여 배양하였고 생장이 적합한 배지는 malt extract agar (MEA), Sabouraud dextrose agar (SDA) 배지보다 potato dextrose agar (PDA)로, 빠른 균사 생장 및 균사 밀도를 보였다. P. edulis 균주의 균사 생육 조건은 PDA에서는 20℃, potato dextrose broth (PDB)에서는 25℃가 선발되었으며, 균사생장에 적합한 수소이온 농도가 PDB는 pH 5~8로 이때 균사생장이 영향을 받지 않았다. 두 균주(NIFoS 2792, 2804)는 PDA의 균사 생장 및 밀도를 기준으로 우수한 균주로 선정되었다. 모든 균주는 셀룰라아제와 라카아제 활성을 나타내었고 NIFoS 2407과 2805는 다른 균주보다 높은 효소 활성을 보였다. 그 중에서도 라카아제 활성은 NIFoS 2387이었고 모든 균주는 셀룰라아제를 생산하였다. 톱밥 종류별 시험에서 상수리나무와 신갈나무에서 균사생장속도가 다른 톱밥에서보다 좋았고 균사 밀도도 가장 양호하였다. 버섯의 톱밥재배는 23℃에서 균 접종 후 80~85일간 배양하였고, 원기형성 온도는 17~18℃에서 10~11일간, 자실체 생육은 15~20일간 수행하였다. 버섯 재배 결과, 배양기간과 수량 면에서 NIFoS 2804, NIFoS 3993 균주가 가장 양호한 균주로 선발되었다. 이러한 결과는 추후 P. edulis의 인공재배를 하는데 유용한 정보로 활용 될 수 있을 것이다.